Comment notre cerveau arrive-t-il à éliminer le parasite qui contrôle l’esprit des rats pour leur faire aimer l’urine des chats ?
Le Guru revient sur certaines actualités scientifiques de la semaine alors qu’il était en pause. Durant son absence, un petit problème de connexion indépendant de sa volonté l’a empêché de modérer les commentaires, ce qui est désormais réalisé… encore désolé !
Pour les néophytes du Guru, celui-ci a un faible pour les parasites… et il y en a un qui se démarque du reste en raison des sa capacité à modifier le comportement de certaines créatures et de la proximité qu’il peut avoir avec l’humain. Il s’agit du Toxoplasma Gondii, un parasite microscopique qui manipule l’esprit des rats pour leur faire aimer l’urine des chats, car ce toxoplasme a besoin des chats pour continuer son développement…
Depuis plus de 10 ans, le Guru vous a gavé d’articles, effrayant pour certains (étude à l’appui), à son sujet…
Ces dernières années, il y a même eu des suspicions qui sont apparues concernant le fait que ce parasite, qui infecte également les humains (toxoplasmose), notamment par l’intermédiaire des excréments du chat, pourrait les “influencer”, exemple :
Mais si la toxoplasmose peut être problématique dans certains cas, elle ne présente aucun symptôme détectable pour la plupart des humains.
À présent, un groupe de chercheurs pense savoir pourquoi, et cela implique que des cellules du cerveau se sacrifient pour tirer la sonnette d’alarme.
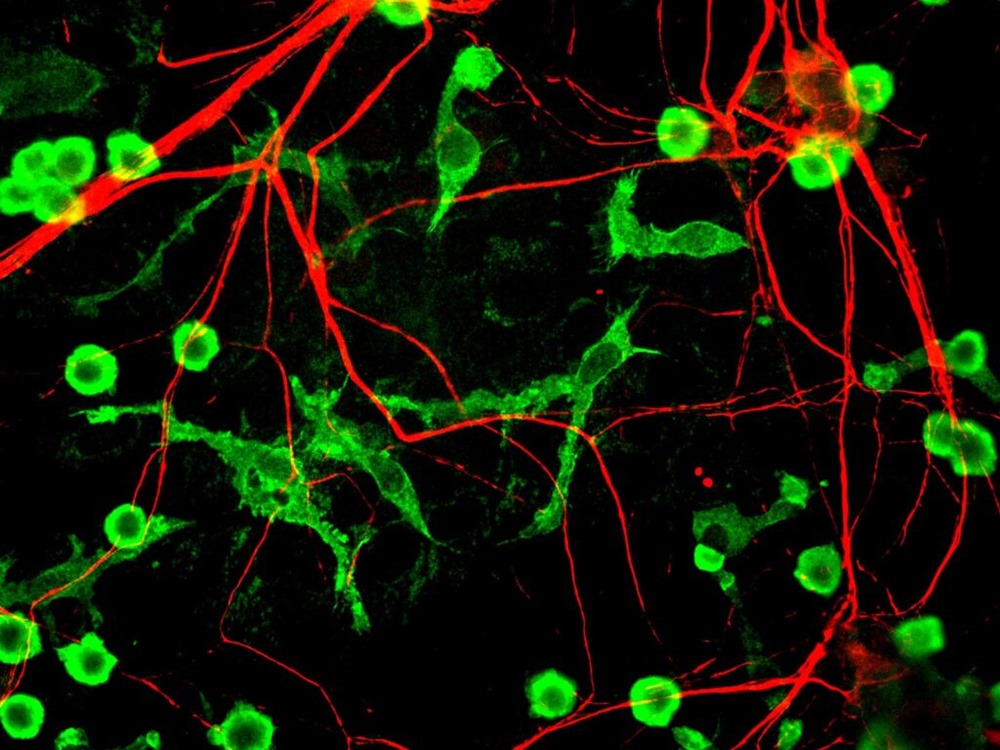
Selon une nouvelle étude, le parasite de la toxoplasmose est maintenu sous contrôle par des cellules immunitaires appelées microglies (microgliocytes). Ce sont les défenseurs et résidents du cerveau, qui agissent comme des macrophages et constituent la principale forme de défense immunitaire du système nerveux central.
Image d’entête : des microglies dans un cerveau humain. (Gerry Shaw)
Ces microglies libèrent également une molécule unique, appelée IL-1α (également appelée interleukine-1 ou hematopoietin 1) qui peut jouer de nombreux rôles, mais dans ce cas, elle est utilisée comme système d’alarme. Les microglies doivent se sacrifier pour sécréter l’IL-1α afin de faire savoir aux autres cellules que quelque chose ne va pas, une découverte qui pourrait avoir des implications pour de nombreuses maladies qui affectent le cerveau, de l’accident vasculaire cérébral à la sclérose en plaques ou aux maladies neurodégénératives.
Pendant des décennies, la croyance populaire prétendait que le cerveau était déconnecté du système immunitaire, mais de récentes recherches ont montré que ce n’était pas le cas. Les microglies sont au centre de ce débat, mais il n’est pas facile de les étudier. Jusqu’à récemment, les équipements de laboratoire avaient du mal à distinguer les microglies du cerveau des autres types de cellules immunitaires. Récemment, Samantha Batista, de l’université de Virginie (Etats-Unis), a utilisé une approche élégante pour étudier ces microglies.
Avec ses collègues, elle a découvert que l’infection provoque l’éclatement des microglies de manière inflammatoire, un processus que les autres cellules immunitaires ne subissent pas. Ils ont utilisé cette approche pour étudier comment les microglies contrôlent l’infection au Toxoplasma gondii. Les personnes ayant un système immunitaire sain n’ont généralement aucun problème à maîtriser l’infection et ne présentent aucun symptôme. Cependant, les personnes immunodéprimées peuvent tomber très malades.
Cette situation est particulièrement “intéressante” pour un certain nombre d’affections selon Batista :
Comprendre des voies comme celle-ci pourrait être bénéfique pour d’autres maladies impliquant une neuroinflammation. Nous pouvons nous demander si la favorisation de cette voie est utile dans les situations où il faut une présence immunitaire plus importante dans le cerveau, comme les infections ou les cancers, et aussi si l’inhibition de cette molécule pourrait être utile dans les maladies provoquées par une trop forte neuroinflammation, comme la sclérose en plaques. Cibler une voie spécifique de ce type pourrait avoir moins d’effets hors cible que de cibler l’inflammation de manière plus générale.
Maintenant que les chercheurs savent comment la microglie tire la sonnette d’alarme, ils se penchent sur la manière dont ils détectent initialement une menace.
Selon M. Harris, qui fait partie du centre d’immunologie Carter de l’université de Virginie :
Le système immunitaire doit pénétrer dans le cerveau pour combattre les infections dangereuses. Nous comprenons maintenant comment les microglies sonnent l’alarme pour protéger le cerveau. Nous soupçonnons que des signaux similaires sont manqués ou mal interprétés dans la maladie d’Alzheimer, ce qui ouvre une nouvelle voie de recherche passionnante en laboratoire.
L’étude publiée dans Nature Communications : Gasdermin-D-dependent IL-1α release from microglia promotes protective immunity during chronic Toxoplasma gondii infection et présentée sur le site de l’université de Virginie : Your Brain Parasite Isn’t Making You Sick. Here’s Why.