Un isotope rare de l’oxygène a enfin été détecté tout en révélant un problème avec les lois de la physique
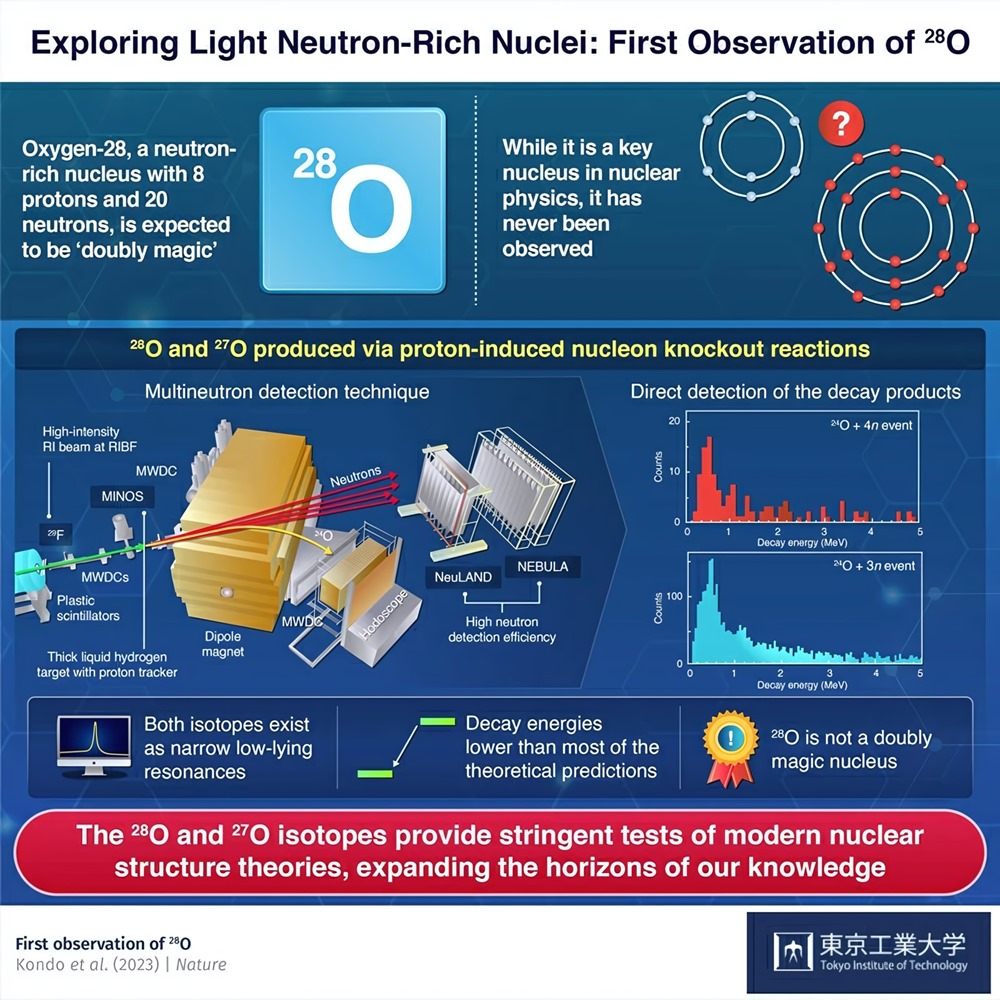
Des scientifiques ont observé une nouvelle forme d’oxygène qui remet en cause de vieilles convictions. Baptisé oxygène-28, cet isotope possède le plus grand nombre de neutrons observé à ce jour dans un atome d’oxygène. Étonnamment, malgré les prévisions de stabilité, il se désintègre rapidement.
Image d’entête : deux exemples d’isotope de l’Oxygène, à gauche l’oxygène-16 et à droite l’oxygène-18. (J. kolf/ Isobar)
Les atomes sont constitués d’un noyau contenant des nucléons, protons et neutrons. Le nombre de protons définit le numéro atomique d’un élément, tandis que le nombre de neutrons peut varier, ce qui donne différents isotopes du même élément. Par exemple, alors que l’oxygène a toujours 8 protons, le nombre de neutrons peut varier.
Avant cette découverte, l’oxygène-26 détenait le record du plus grand nombre de neutrons (18). Cependant, sous la direction de Yosuke Kondo, de l’Université de technologie de Tokyo, les scientifiques ont découvert deux isotopes de l’oxygène jamais vus auparavant : l’oxygène-27 et l’oxygène-28, qui possèdent respectivement 19 et 20 neutrons.
Le RIKEN Radioactive Isotope Beam Factory, au Japon, a servi de cadre à l’expérience. Les scientifiques y ont tiré des isotopes de calcium-48 sur une cible de béryllium, produisant ainsi des atomes plus légers comme le fluor-29. Cet isotope de fluor unique a ensuite été soumis à une collision avec de l’hydrogène liquide, ce qui a permis d’obtenir l’oxygène-28 attendu.
Le Riken RI Beam Factory de Wako, au Japon, crée des flux d’isotopes radioactifs avec l’aide de ce cyclotron annulaire supraconducteur. (Nishina Center for Accelerator-Based Science)
L’oxygène-27 et l’oxygène-28 se sont révélés éphémères, se désintégrant rapidement en oxygène-24 avec quelques neutrons égarés. Mais il y a un hic : traditionnellement, 8 et 20 sont considérés comme des “nombres magiques”, ce qui implique que l’oxygène-28 devrait faire preuve de stabilité.
En physique nucléaire, les nombres magiques correspondent à des nombres de nucléons qui complètent une enveloppe, séparés par des écarts d’énergie substantiels. Les noyaux contenant des enveloppes/ couches de protons et de neutrons remplies par ces nombres sont considérés comme « doublement magiques » et sont donc stables. L’oxygène prédominant de notre atmosphère, l’oxygène 16, répond à ce critère doublement magique.
Résumé graphique de l’étude. (Kondo et col./ Nature)
Pendant des années, on a cru que l’oxygène-28 était l’isotope d’oxygène doublement magique qui succédait à l’oxygène-16, mais il est resté introuvable. Aujourd’hui, les découvertes de l’équipe de Kondo présentent une raison convaincante : l’enveloppe de neutrons n’était pas complète, ce qui jette le doute sur le fait que 20 soit un nombre magique.
Les observations actuelles entrent en résonance avec un autre phénomène particulier observé dans les isotopes du néon, du sodium et du magnésium. Dans ces cas, l’enveloppe de 20 neutrons ne se scelle pas. L’anomalie s’étend également au fluor-29 et, de toute évidence, à l’oxygène-28.
Pour approfondir le mystère de cette couche neutronique, il est nécessaire d’effectuer des recherches plus approfondies sur l’état énergétique du noyau. La découverte d’autres méthodes de production de l’oxygène-28 pourrait apporter des éclaircissements supplémentaires, bien que cela reste une entreprise difficile.
L’équipe de Kondo a jeté les bases qui permettront de comprendre de manière révolutionnaire les noyaux doublement magiques, révélant ainsi certaines complexités du monde atomique.
L’étusde publiée dans Nature : First observation of 28O et présentée sur le site de l’Université de technologie de Tokyo : Exploring Light Neutron-Rich Nuclei: First Observation of Oxygen-28.