Nous savons enfin comment les tardigrades sont pratiquement invincibles face aux conditions extrêmes
Pour la première fois, des scientifiques ont découvert le mécanisme moléculaire précis qui confère au tardigrade, l’un des organismes les plus résistants de la planète, la rare capacité d’activer une cape de quasi-invincibilité lorsqu’il est confronté à un stress extrême.
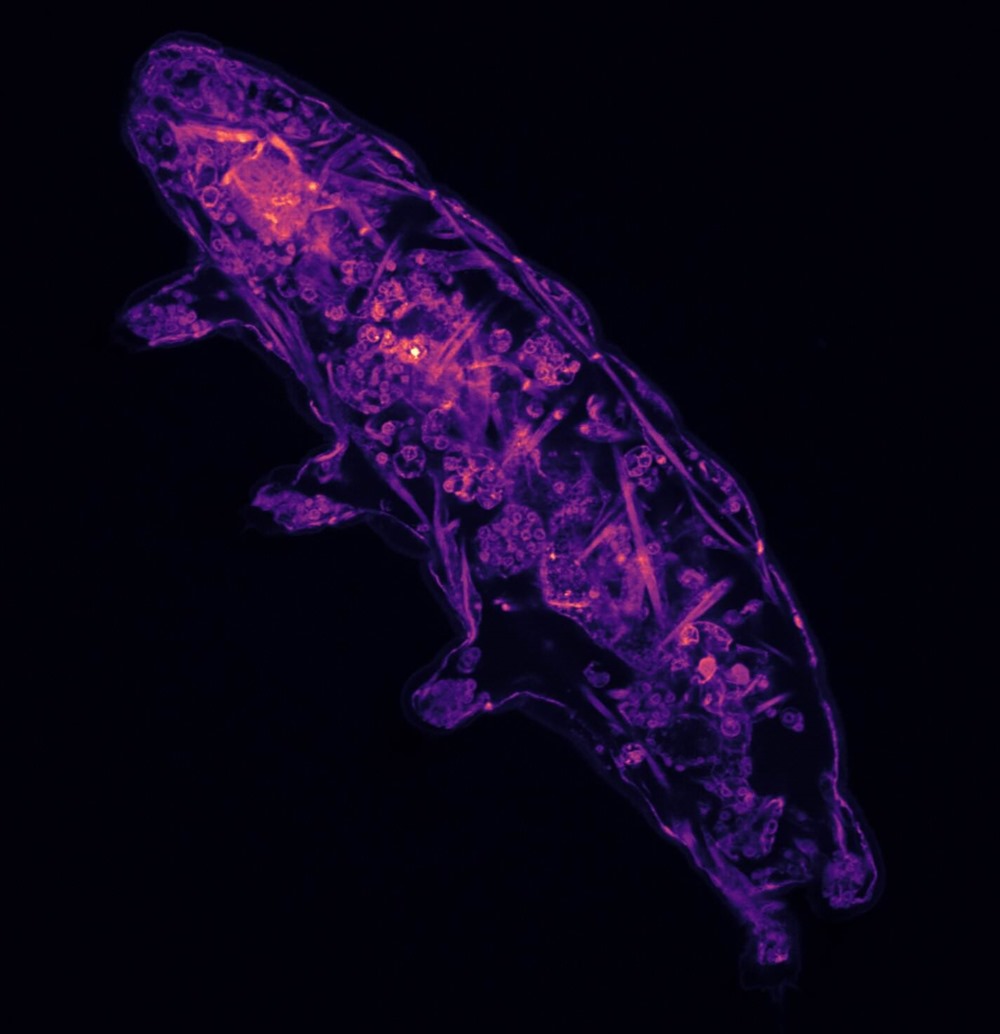
Image d’entête : un tardigrade vu au microscope à fluorescence, avec un marqueur fluorescent mettant en évidence certains de ses organes. (Smythers et col./ PLoS ONE)
Ces invertébrés aquatiques à huit pattes sont bien connus pour leur capacité à résister à la chaleur intense, au froid et à la sécheresse, entrant dans un état de déshydratation connu sous le nom de “tun”, le tardigrade microscopique se rétrécissant à un tiers de sa taille déjà petite et se mettant en boule. Dans cet état de dormance au métabolisme extrêmement lent, une forme de cryptobiose appelée anhydrobiose, l’animal peut vivre pendant de longues périodes, avant de sortir de son hibernation pour reprendre ses activités normales.
Une précédente étude avait permis de découvrir les processus biologiques à l’origine de cet état d’animation suspendue, mais ce qui le déclenchait restait un mystère. À présent, une équipe dirigée par des chercheurs de l’université de Caroline du Nord à Chapel Hill et de l’université Marshall (Etats-Unis) a identifié l’interrupteur moléculaire qui déclenche la transformation du tardigrade.
Les scientifiques ont exposé une espèce modèle de tardigrade, l’Hypsibius exemplaris, à des conditions extrêmes, des températures de congélation de -80 °C, des niveaux élevés de peroxyde d’hydrogène et des solutions salines et sucrées fortes, afin de déclencher la transformation en tun. Ils ont découvert qu’un capteur moléculaire construit sur l’acide aminé cystéine était la clé de la capacité de l’animal à activer et désactiver cet état en fonction des besoins.
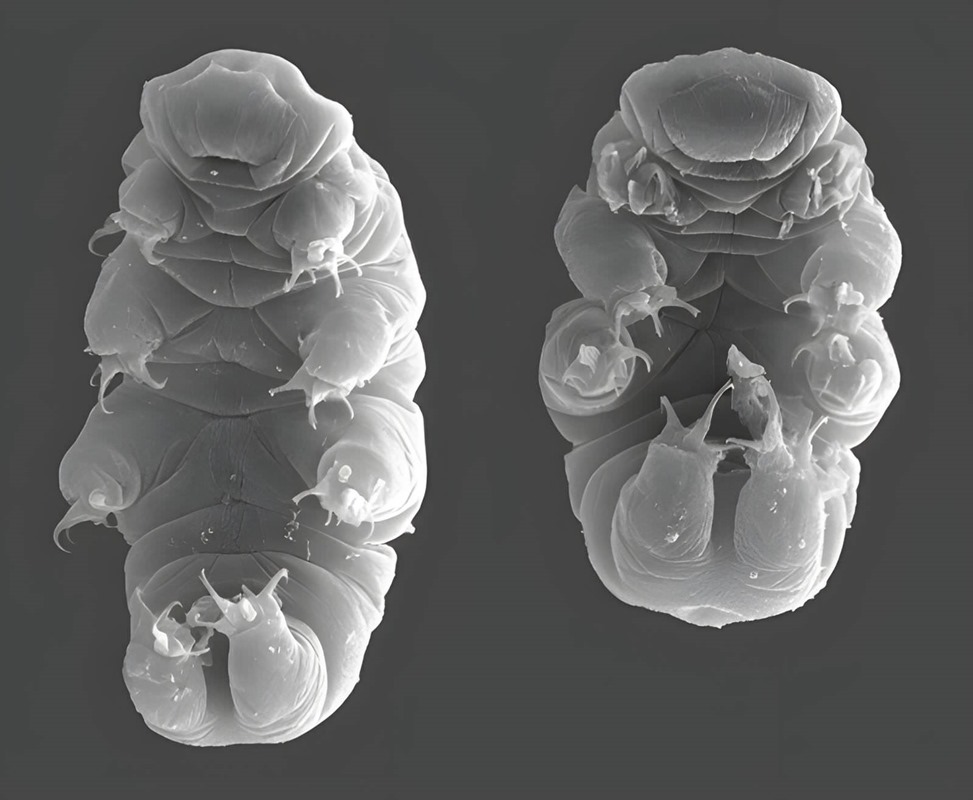
Deux tardigrades Hypsibius exemplaris, sous un microscope électronique à balayage. (Willow Gabriel/ Goldstein lab – tardigrades)
Dans ces conditions extrêmes, les tardigrades présentent une accumulation de radicaux libres, atomes ou molécules d’oxygène, à l’intérieur des cellules, qui volent des électrons à d’autres atomes. À forte concentration, les radicaux libres provoquent un stress oxydatif important, mais pour les tardigrades, ils agissent comme un déclencheur de l’anhydrobiose.
Lorsque l’environnement est redevenu plus hospitalier, ce processus s’est inversé et le tardigrade a reçu le message moléculaire qu’il pouvait revenir à son état d’origine, c’est-à-dire à son état de fonctionnement complet.Cependant, lorsque les scientifiques ont bloqué la cystéine chez les animaux, ceux-ci ont été incapables d’entrer dans leur état de dormance salvateur, révélant ainsi l’interaction importante entre la combinaison des radicaux libres de l’oxygène et ce « commutateur » d’acide aminé.
Selon les chercheurs dans leur étude :
Nous avons révélé que la survie des tardigrades dépend des cystéines oxydées de manière réversible qui coordonnent l’entrée et la sortie des états de survie d’une manière hautement régulée. « Grâce à la mise en œuvre de cribles EPR et de bibliothèques redox, nous avons démontré que la libération intracellulaire de ROS est essentielle pour la formation de tun.
L’étude publiée dans PLOS One : Chemobiosis reveals tardigrade tun formation is dependent on reversible cysteine oxidation.