Une bactérie a évolué vers une nouvelle structure cellulaire à l’intérieur d’algues
Les bactéries autrefois libres n’ont fusionné avec d’autres organismes qu’à trois reprises au cours des 3,5 milliards d’années qui se sont écoulées depuis l’apparition de la vie sur Terre, ce qui en fait un événement de l’évolution extrêmement rare. À présent, un quatrième exemple a été découvert, chez une algue unicellulaire répandue dans les océans.
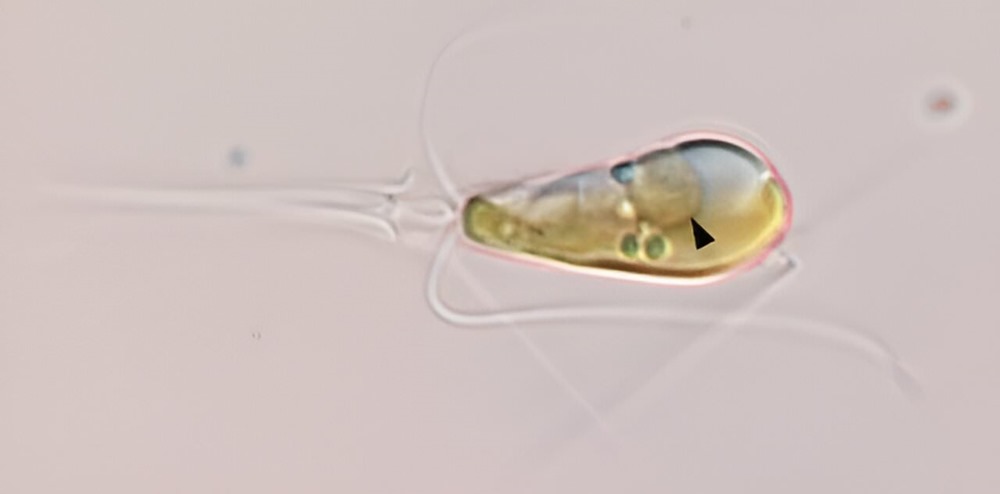
Image d’entête : cellule de la bactérie Braarudosphaera bigelowii, avec une flèche noire montrant son organite fixateur d’azote. ( Tyler Coale/ Université de Californie à Santa Cruz)
Il était admis que ces algues « fixaient » l’azote, c’est-à-dire le transformaient en ammoniac utilisable, avec l’aide d’une bactérie. Tyler Coale, de l’université de Californie à Santa Cruz, et ses collègues viennent de montrer que cette bactérie a évolué vers une nouvelle structure cellulaire, ou organite. Il s’agit du premier organite fixateur d’azote connu, ou “nitroplaste”, selon Coale, et il pourrait être la clé du succès de ces algues, il ajoute :
Il semble que ce soit une stratégie fructueuse pour elles. Ces algues sont très répandues. On les trouve dans tous les océans du monde.
Les manuels de biologie modernes affirment que seules les bactéries peuvent prélever de l’azote dans l’atmosphère et le convertir en une forme utilisable pour la vie. Les plantes qui fixent l’azote, comme les légumineuses, le font en hébergeant des bactéries symbiotiques dans les nodules des racines. Mais cette découverte récente bouleverse cette règle.
Il est assez fréquent qu’une espèce vive à l’intérieur des cellules d’une autre espèce dans le cadre d’une relation mutuellement bénéfique appelée endosymbiose. Par exemple, les cellules des racines des légumineuses telles que les pois hébergent des bactéries fixatrices d’azote. La réussite des cafards est en partie due à des bactéries endosymbiotiques qui produisent des nutriments essentiels. Certaines cellules hébergent même plusieurs endosymbiontes.
Si les relations endosymbiotiques peuvent devenir très étroites, dans presque tous les cas, les organismes restent distincts. Par exemple, les légumineuses acquièrent leurs bactéries racinaires à partir du sol. Et si les bactéries de la blatte sont transmises par les œufs, elles vivent dans des cellules spécialisées et non dans toutes les cellules. Mais dans trois cas, les endosymbiotes ont fusionné avec leurs hôtes pour en devenir un élément fondamental.
Les mitochondries productrices d’énergie sont nées de la fusion d’une bactérie avec une autre cellule simple, formant les cellules complexes qui ont donné naissance aux animaux, aux plantes et aux champignons. Les plantes sont nées de la fusion d’une cyanobactérie avec une cellule complexe pour former le chloroplaste, l’organite qui réalise la photosynthèse. Il y a environ 60 millions d’années, une autre cyanobactérie a fusionné avec une amibe, formant un organite photosynthétique différent appelé chromatophore, que l’on ne trouve que chez quelques espèces de Paulinella (le genre d’au moins onze espèces comprenant des amibes d’eau douce et d’eau de mer).
On soupçonne depuis plus d’une décennie qu’une cyanobactérie connue sous le nom d’UCYN-A (Atelocyanobacterium thalassa) et vivant dans l’algue unicellulaire Braarudosphaera bigelowii est devenue un organite.
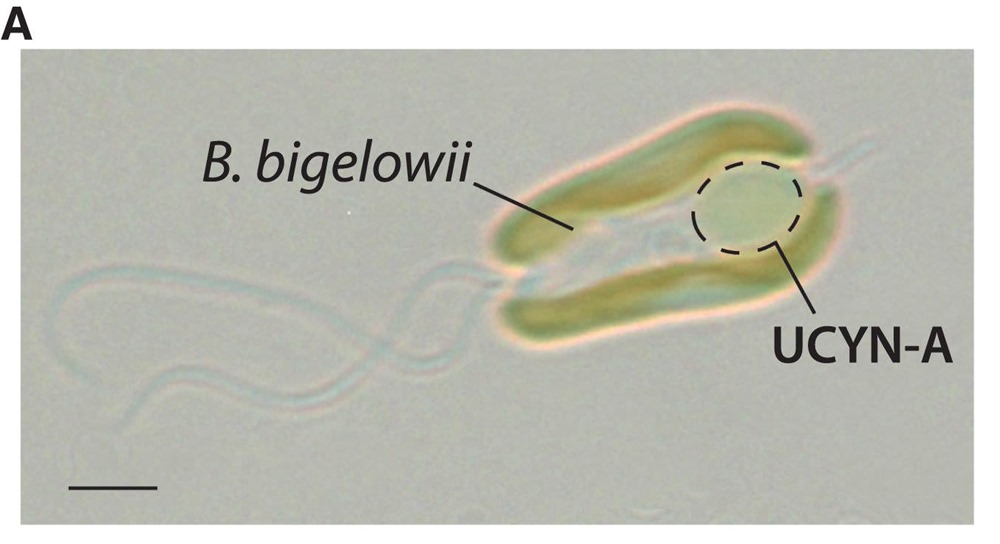
Image au microscope optique de la B. bigelowii en symbiose avec l’UCYN-A (échelle, 2 μm ; image reproduite avec l’aimable autorisation de Wing Kwan Esther Mak et Kyoko Hagino). (F. Cornejo-Castillo et col. Cell)
 Toutefois, l’étude de ce partenariat était difficile jusqu’à ce que Kyoko Hagino, membre de l’équipe de l’université de Kochi au Japon, trouve le moyen de maintenir la B. bigelowii en vie en laboratoire. Cela a permis à l’équipe d’utiliser une technique appelée “soft X-ray tomography” (tomographie douce à rayons X) pour observer ce qui se passe lorsque les cellules de l’algue se divisent. Cette technique a permis de découvrir que l’UCYN-A se divise de concert avec la cellule algale, chaque cellule fille héritant d’une UCYN-A.
Toutefois, l’étude de ce partenariat était difficile jusqu’à ce que Kyoko Hagino, membre de l’équipe de l’université de Kochi au Japon, trouve le moyen de maintenir la B. bigelowii en vie en laboratoire. Cela a permis à l’équipe d’utiliser une technique appelée “soft X-ray tomography” (tomographie douce à rayons X) pour observer ce qui se passe lorsque les cellules de l’algue se divisent. Cette technique a permis de découvrir que l’UCYN-A se divise de concert avec la cellule algale, chaque cellule fille héritant d’une UCYN-A.
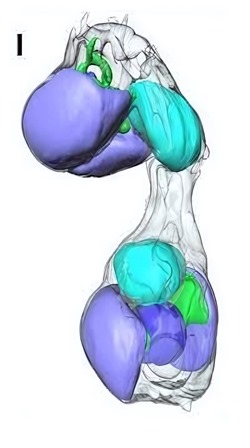
Ci-contre : une image de tomographie douce aux rayons X montre la division cellulaire de B. bigelowii, avec les nitroplastes (UCYN-A) en cyan. (Valentina Loconte/ Université de Californie à Santa Cruz)
Selon Coale :
Nous ne savions pas comment cette association s’opérait entre l’UCYN-A et la cellule algale. Auparavant, nous ne savions pas comment cette association était maintenue.
L’équipe a également constaté qu’environ la moitié des quelque 2 000 protéines différentes contenues dans l’UCYN-A proviennent de l’algue hôte, au lieu d’être fabriquées par l’UCYN-A elle-même. Un grand nombre des protéines importées aident l’UCYN-A à fixer l’azote, explique Coale qui ajoute :
Je pense que la cellule de l’algue l’aide à produire plus d’azote qu’elle n’en a besoin pour elle-même.
Il semble également exister un système spécialisé de livraison des protéines à l’UCYN-A, comme c’est le cas pour d’autres organites. Toutes les protéines importées comportent une section supplémentaire, considérée comme une « étiquette d’adresse », qui indique qu’elles doivent être livrées à l’UCYN-A. Il n’existe pas de définition universellement acceptée d’un organite, mais de nombreux biologistes considèrent que la division coordonnée et l’importation de protéines sont essentielles.
La fabrication et l’utilisation d’engrais azotés constituent une source majeure d’émissions de gaz à effet de serre ainsi qu’une dépense pour les agriculteurs. Il y a donc un grand intérêt à modifier les plantes cultivées pour qu’elles puissent fixer leur propre azote, comme le font les légumineuses. L’un des moyens d’y parvenir serait d’équiper leurs cellules de “nitroplastes” et Jeff Elhai de l’Université du Commonwealth de Virginie a élaboré une proposition à cet effet. Mais l’UCYN-A n’est pas un bon point de départ, car elle est beaucoup trop dépendante de la B. bigelowii, explique-t-il.
Elhai envisage plutôt de commencer par des cyanobactéries qui viennent à peine de commencer à devenir des nitroplastes et qui ne dépendent pas de protéines importées, de sorte qu’elles pourraient être facilement ajoutées à un large éventail de plantes cultivées.
Néanmoins, Elhai est d’accord avec Coale pour dire que l’étude de B. bigelowii pourrait nous aider à comprendre comment intégrer la fixation de l’azote dans une cellule végétale.
Les études publiées dans Science :
et dans Cell : Metabolic trade-offs constrain the cell size ratio in a nitrogen-fixing symbiosis et présentées sur le site de l’Université de Californie à Santa Cruz : Scientists discover first nitrogen-fixing organelle.