Chez les souris, des spermatozoïdes empoisonnent leurs voisins pour arriver les premiers
Quand les spermatozoïdes font la course, c’est pour gagner. Il n’est donc pas surprenant que chez certaines espèces, la compétition pour savoir qui atteint l’ovule en premier puisse être un peu salissante…
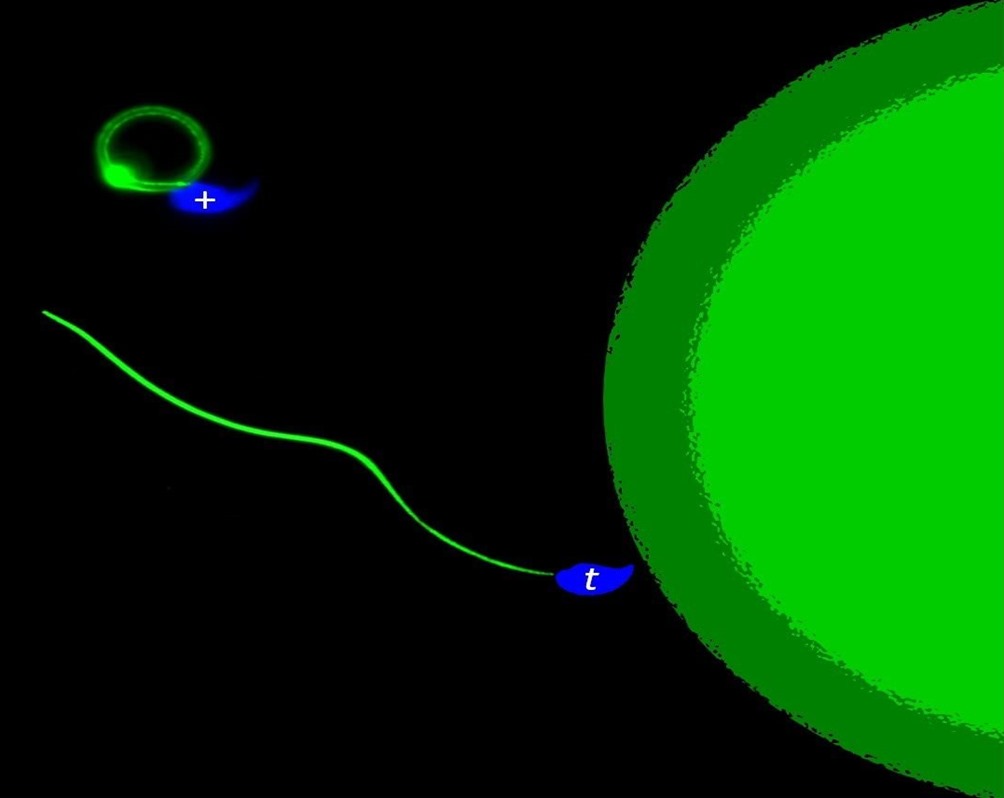
Image d’entête : en compétition directe, les spermatozoïdes t surpassent leurs pairs normaux (+) dans la course à l’ovule par des astuces génétiques, les laissant nager en rond. (MPI f. Molecular Genetics/ Alexandra Amaral)
On a découvert qu’une variante de gènes de la souris donne aux spermatozoïdes qui la possèdent un net avantage en empoisonnant leurs voisins pendant leur développement, les privant ainsi de leur capacité à repérer efficacement leur chemin vers l’ovule.
Une course composée uniquement de ces “assassins” en puissance serait un désastre complet, les chercheurs ayant découvert que la variante génétique risque un surdosage de son propre cocktail mortel, à moins que la course ne soit compensée par ses victimes.
Les généticiens de l’Institut Max Planck de génétique moléculaire à Berlin (Allemagne) ont découvert ce « code (génétique) de triche » plutôt unique dans le sperme de souris tout en étudiant les mécanismes utilisés par les cellules sexuelles mâles pour se frayer un chemin dans le système reproductif féminin.
Selon le directeur de l’institut, Bernhard Herrmann :
Nos données mettent en évidence le fait que les spermatozoïdes sont des concurrents impitoyables.
Les différences génétiques peuvent donner à un seul spermatozoïde un avantage dans la course à la vie, favorisant ainsi la transmission de variantes génétiques particulières à la génération suivante.
Ils ont découvert qu’un “interrupteur” de la protéine Rho (Protéine G) appelé RAC1 joue un rôle essentiel dans le maintien du sperme sur la bonne voie. Si vous touchez à ce régulateur, les spermatozoïdes vont tituber comme s’ils rentraient chez eux après l’heure de fermeture des bars (hors confinement…).
Mais apparemment, l’évolution a tout arrangé. Selon les chercheurs, une variation du codage des séquences sur le chromosome 17 semble y remédier, en fabriquant un produit qui entrave les activités de RAC1.
Cette région, appelée t-variant, n’est pas nouvelle pour la science. En fait, cette partie de l’ADN est une bizarrerie de la génétique mendélienne depuis près d’un siècle.
Les souris hétérozygotes pour ce trait (ayant un chromosome 17 t-variant et un chromosome partenaire avec un chromosome « normal ») n’engendrent pas le ratio 50-50 de la progéniture auquel on pourrait s’attendre. Les chances qu’un de leurs descendants naisse sans la variante t sont en fait de 1 sur 100. Mais s’i elles sont homozygotes, les deux versions du chromosome 17 contenant ce chromosome anormal, elles peuvent alors dire adieu à la paternité. Elles sont complètement stériles.
En gardant tout cela à l’esprit, les chercheurs ont découvert ce qui se passe à l’intérieur des testicules de ces petites souris en effectuant le génotypage de chaque spermatozoïde et en évaluant leur motilité.
Au début de la production de gamètes, à l’intérieur des cellules précurseurs du sperme qui contiennent à la fois le chromosome t-variant et une version plus normale, le code-t toxique interfère avec le développement de la RAC1, la rendant ainsi inopérant.
Cependant, une fois que les cellules précurseurs se sont finalement divisées en leurs formes spermatiques, elles subissent le processus de méiose, divisant les chromosomes de sorte que chaque spermatozoïde ne possède qu’un seul de chaque paire.
Cela signifie que certains spermatozoïdes ont maintenant un chromosome t-variant, et d’autres non. Voici la partie vraiment astucieuse : les t-variants produisent également leur propre remède, sauvant RAC1 du danger en exprimant une protéine régulatrice spécifique.
Selon Herrmann :
Imaginez un marathon, où tous les participants reçoivent de l’eau potable empoisonnée, mais où certains coureurs prennent aussi son antidote.
Cet antidote fonctionne bien à des doses suffisamment faibles. Malheureusement, l’abondance de RAC1 est tout aussi néfaste qu’un manque. Dans un marathon rempli d’empoisonneurs produisant tous des antidotes, les coureurs seront bientôt accablés par un excès de RAC1.
Selon Alexandra Amaral, l’auteur principal de l’étude :
La compétitivité des spermatozoïdes individuels semble dépendre d’un niveau optimal de RAC1 actif ; une activité réduite ou excessive de RAC1 interfère avec une progression efficace.
C’est la première fois que des expériences ont précisément démontré comment des souris t-variant hétérozygotes obtiennent un avantage, tout en affirmant la biochimie de la RAC1 dans la navigation du sperme des mammifères.
Étant observée chez les souris, la recherche n’a qu’une portée limitée sur la reproduction humaine. Mais plus nous en savons sur les divers modèles de chimie de la reproduction dans le règne animal, mieux nous comprenons comment la nôtre a évolué.
L’étude publiée dans PLOS One : RAC1 controls progressive movement and competitiveness of mammalian spermatozoa et présentée sur le site de l’Institut Max-Planck de génétique moléculaire : Some sperms poison their competitors.