Les premiers signes de douleur chronique chez les insectes pointent vers une profonde origine chez l’humain
Les médicaments que nous avons mis au point pour nous aider à traiter la douleur chronique visent en grande partie à supprimer ses symptômes plutôt qu’à éliminer ses causes sous-jacentes. En étudiant le fonctionnement de la douleur chez des mouches des fruits (Drosophile) blessées, les scientifiques ont pour la première fois mis en évidence que ses effets peuvent être durables, ce qui, selon eux, ouvre de nouvelles possibilités de traitements plus efficaces chez l’humain.
Image d’entête : mouche des fruits (Drosophila). (Katja Schulz/ Flickr)
Selon Greg Neely, professeur agrégé à l’université de Sydney, en Australie, qui a dirigé la recherche :
Les gens ne considèrent pas vraiment les insectes comme une source de douleur. Mais il a déjà été démontré chez de nombreux animaux invertébrés différents qu’ils peuvent détecter et éviter les stimuli dangereux que nous percevons comme douloureux. Chez les non-humains, nous appelons ce sens « nociception« , le sens qui détecte les stimuli potentiellement nocifs comme la chaleur, le froid ou les blessures physiques, mais pour simplifier, nous pouvons nous référer à ce que les insectes expérimentent comme « douleur ».
Les mouches des fruits servent souvent de modèles dans ce genre d’études parce qu’elles possèdent des génomes beaucoup plus petits et plus simples que ceux d’autres animaux, que les scientifiques peuvent “bricoler” pour comprendre différents comportements et troubles chez les humains. Par le passé, des scientifiques les ont alcoolisé pour comprendre pourquoi la gueule de bois se produit et ils ont étudié certaines protéines des mouches des fruits qui pourraient nous aider à vivre plus longtemps et en meilleure santé.
Les scientifiques ont appris pour la première fois en 2003 que les mouches des fruits pouvaient ressentir quelque chose qui ressemblait à de la douleur, mais les preuves ne faisaient allusion qu’à un inconfort de courte durée. Des scientifiques de l’université de Sydney ont de nouveau enrôlé l’insecte ailé pour tenter de percer les mystères de la douleur humaine, cette fois-ci en produisant ce qu’ils disent être la première preuve génétique de douleur chronique, qui dure donc longtemps après la guérison de la blessure initiale.
Toujours selon Neely :
Nous savions donc que les insectes pouvaient sentir la douleur, mais ce que nous ne savions pas, c’est qu’une blessure pouvait entraîner une hypersensibilité de longue durée à des stimuli normalement non douloureux, de la même façon que l’expérimentent des patients humains.
Pour en arriver à cette conclusion, Neely et son équipe ont endommagé un nerf dans une patte d’une mouche des fruits et l’ont laissé cicatriser. Bien que la douleur aiguë soit passée, les chercheurs ont découvert que les autres pattes de la mouche étaient aussi devenues hyper sensibles. Des recherches plus poussées ont permis d’en déterminer les raisons grâce à ce que les chercheurs appellent des “freins antidouleur”, qui résident dans ce qui représente la moelle épinière (cordon nerveux ventral) de la mouche et contrôlent le flux des signaux de douleur à travers son corps.
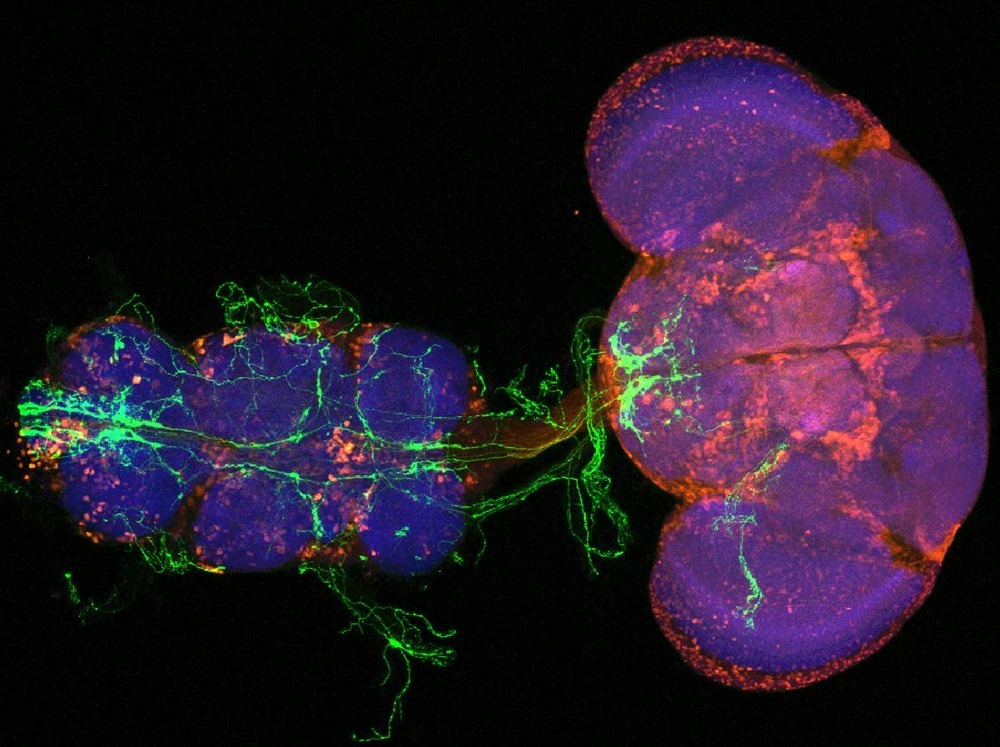
Cerveau et cordon nerveux ventral (ressemblant à la moelle épinière chez l’Homme) d’une mouche présentant des neurones sensoriels nociceptifs (verts), colorés avec un anti-GABA, un neurotransmetteur inhibiteur (rouge) et un marqueur synaptique neuronal nc82 (bleu).
Selon Neely :
Après la blessure, le nerf blessé jette toute sa cargaison dans le cordon nerveux et annihile tous les freins, pour toujours. Alors le reste de l’animal n’a pas de freins sur sa ‘douleur’. Le seuil de la douleur change et maintenant ils sont hypervigilants.
Chez l’homme, un état d’hypervigilance peut se traduire par une sensibilité soutenue et accrue à la douleur, ce qui entraîne une douleur chronique. Cette recherche s’est concentrée sur une forme, appelée douleur neuropathique (ou douleur neurogène), qui résulte d’une atteinte du système nerveux (la douleur inflammatoire est l’autre type de douleur chronique). Les chercheurs pensent que des mécanismes de “freinage” similaires pourraient être en jeu lorsqu’il s’agit de douleur neuropathique chez les humains, mais d’une manière différente.
L’animal relâche ces freins antidouleur comme mécanisme de survie en réponse à des situations dangereuses, mais lorsque les freins sont desserrés chez les humains, cela les condamne à un inconfort soutenu. Heureusement, cette recherche ouvre de nouvelles possibilités quant à la façon dont nous pourrions les remettre en place.
Il est important de noter que nous savons maintenant que l’étape critique qui cause la » douleur » neuropathique chez les mouches, les souris et probablement les humains est la perte des freins de la douleur dans le système nerveux central, nous nous concentrons sur la mise au point de nouveaux traitements ou médicaments à base de cellules souches qui visent la cause sous-jacente et mettent fin définitivement à la douleur.
L’étude publiée dans Science Advances : Nerve injury drives a heightened state of vigilance and neuropathic sensitization in Drosophila et présentée sur le site de Université de Sydney : Thwack! Insects feel chronic pain after injury.