Des cellules de peau utilisées pour produire le premier modèle complet d’embryon humain précoce
Les chercheurs ont très peu de possibilités d’étudier les premiers stades du développement humain, mais une découverte révolutionnaire menée par une équipe australienne va leur fournir un nouveau modèle utile pour étudier la science derrière des questions telles que l’infertilité et les maladies congénitales. En utilisant des cellules de peau comme point de départ, les chercheurs ont produit le premier modèle complet d’un embryon humain précoce, ce qui, selon eux, ouvre de nouvelles possibilités pour la recherche sur la fécondation in vitro et les nombreux facteurs qui peuvent avoir un impact sur les premières étapes importantes de la vie humaine.
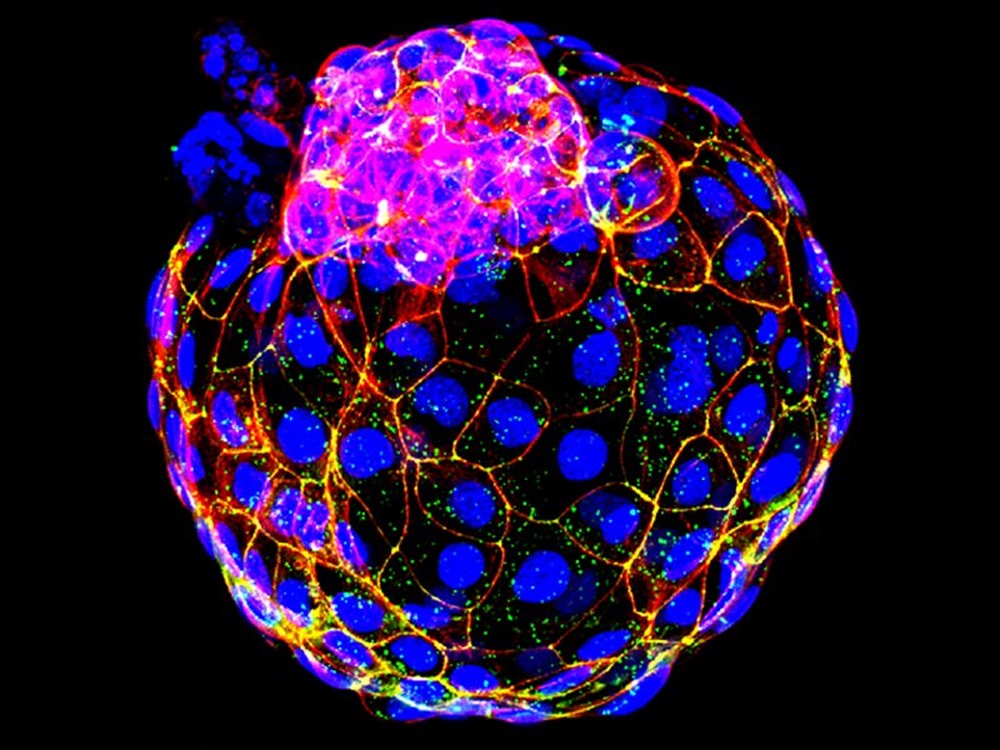
Image d’entête : blastocyste artificiel produit à partir de cellules souches humaines. (École médicale du Sud-Ouest de l’université du Texas)
La recherche a été menée par des scientifiques de l’université Monash en Australie et porte sur ce que l’on appelle les blastocystes humains. Il s’agit de structures formées dans les premiers jours suivant la fécondation, lorsque les cellules se divisent et se rassemblent en une structure tridimensionnelle composée d’un amas interne et d’une couche externe protectrice.
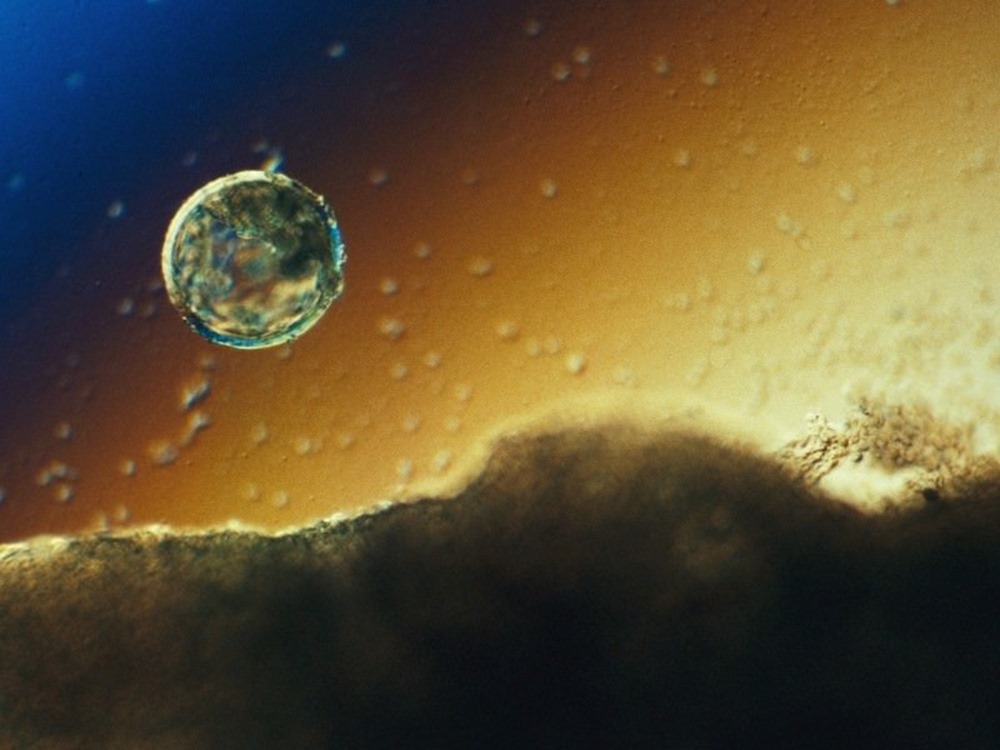
Un blastocyste s’implante dans la paroi de l’utérus vers le septième ou le huitième jour du développement humain. (Lennart Nilsson/ TT/ SPL)
Cependant, l’étude de ce stade précoce et critique du développement embryonnaire s’est avérée difficile, la disponibilité des embryons humains étant limitée et des problèmes éthiques et juridiques se posant. Les auteurs de la nouvelle étude ont donc cherché à savoir comment des versions artificielles créées en laboratoire peuvent fournir un modèle d’étude qui contourne ces problèmes, grâce à ce que l’on appelle la reprogrammation nucléaire.
Cette technique consiste à modifier l’expression génétique d’un type de cellule pour qu’elle adopte le comportement d’une autre, en l’exposant à un nouvel environnement et à des facteurs de croissance. Dans ce cas, les chercheurs ont pris des cellules de peau humaine et les ont placées dans un échafaudage gélatineux, les reprogrammant en éléments constitutifs d’un blastocyste, qui s’est ensuite organisé selon la structure souhaitée.
Animation expliquant la recherche sur les iBlastoïdes : des cellules de peau humaine sont reprogrammées par un cocktail de facteurs de reprogrammation (RF). Pendant la reprogrammation, elles sont ensuite placées dans des micropuits en forme de V, où elles se transforment progressivement en une structure cellulaire 3D semblable à un blastocyste, appelée iBlastoïde. (Monash Biomedicine Discovery Institute)
Les blastocystes artificiels de l’équipe, qu’ils ont baptisés iBlastoïdes, ne sont pas identiques aux blastocystes naturels. Il leur manque une membrane externe, appelée zone pellucide, et ils ont du mal à se développer au-delà des premiers jours. Ce point est important, car il permet aux recherches de l’équipe de respecter les directives internationales qui stipulent que les blastocystes humains ne peuvent être cultivés au-delà du 14e jour, lorsqu’une structure transitoire appelée « strie primitive » se développe. C’est ce qu’on appelle la « règle de la strie primitive » (primitive streak rule).
Les iBlastoïdes présentent néanmoins suffisamment de similitudes structurelles pour constituer un modèle complet d’embryon humain. Ils comportent une masse interne et une couche externe de cellules ainsi qu’une cavité intérieure, reflétant la génétique et l’architecture globales de leurs homologues naturels.
Vidéo de laboratoire des iBlastoïdes, avec la structure de type trophectoderme en bleu et la structure de type masse cellulaire interne en jaune. (Monash Biomedicine Discovery Institute)
Selon le professeur Jose Polo de l’université Monash :
Les iBlastoïdes permettront aux scientifiques d’étudier les toutes premières étapes du développement humain et certaines des causes de l’infertilité, des maladies congénitales et de l’impact des toxines et des virus sur les embryons précoces, sans avoir recours aux blastocystes humains et, surtout, à une échelle sans précédent, ce qui accélérera notre compréhension et le développement de nouvelles thérapies.
L’étude publiée dans Nature : Modelling human blastocysts by reprogramming fibroblasts into iBlastoids et présentée sur le site de l’université Monash : Australian-led international research team generates the first model of early human embryos from skin cells.