Après le mammouth laineux, des scientifiques veulent maintenant ressusciter l’emblématique tigre de Tasmanie

Le thylacine (Thylacinus cynocephalus), communément appelé tigre de Tasmanie, était un animal très particulier. Il ressemblait à un chien ou à un loup avec les rayures d’un tigre, tout en étant un marsupial. C’est le genre de mélange insolite dont peu d’endroits autres que l’Australie peuvent se vanter.
L’histoire du déclin du thylacine est intrinsèquement liée à celle de l’humain. Dès que les premiers chasseurs-cueilleurs sont entrés en scène, le thylacine a eu de gros problèmes. Au fur et à mesure que l’humain étendait son influence sur le continent, l’aire de répartition du marsupial n’a fait que décliner. Lorsque l’homme a introduit le dingo (Canis lupus dingo) en Australie, il y a plusieurs milliers d’années, le thylacine a presque été exterminé par la concurrence. Mais on pouvait encore trouver une population isolée en Tasmanie, qui n’a cependant pas survécu.
Au XIXe siècle, les colons européens considéraient les prédateurs marsupiaux comme des nuisibles pour leurs moutons. Ils versèrent une prime de 1 £ par carcasse (une bonne somme à l’époque), ce qui entraina le thylacine au bord de l’extinction. En 1909, les primes ont été abandonnées, mais il était déjà trop tard. Il ne restait que quelques individus à l’état sauvage, qui furent saisis par des zoos. Le 7 septembre 1936, le dernier tigre de Tasmanie est mort dans un zoo de Hobart, en Australie.
Une vidéo du tigre de Tasmanie. Des images redécouvertes en 2020 par des chercheurs du groupe Facebook Tasmanian Tiger Archives collaborant avec la State Library and Archive (Australie).
En 2021, Colossal Biosciences, une startup américaine de génie génétique fondée par l’entrepreneur technologique Ben Lamm et le professeur de génétique de Harvard George Church, a annoncé son projet ambitieux de redonner vie au mammouth laineux à l’aide d’une technologie d’édition génétique de pointe telle que CRISPR.
Plus tôt cette année, la société de biotechnologie basée à Dallas a reçu un financement de 60 millions de dollars, dirigé par Thomas Tull et At One Ventures. Aujourd’hui, la startup a annoncé qu’elle allait se lancer dans une deuxième mission, celle de ramener le thylacine d’entre les morts.
À cette fin, Colossal s’est associée à l’Université de Melbourne (Australie) et à son laboratoire de recherche sur la restauration génétique intégrée des thylacines, dirigé par le Dr Andrew Pask. En 2017, Pask et ses collègues ont séquencé pour la première fois le génome du thylacine à partir d’un petit thylacine mort en 1909 et conservé depuis dans l’alcool. Cette analyse a montré que l’espèce éteinte est plus apparentée au kangourou qu’au dingo, parmi de nombreux autres éléments comme une forte baisse de la diversité génétique correspondant à une chute de la population qui a commencé il y a environ 70 000 à 120 000 ans, bien avant l’arrivée des humains sur le continent australien.
Le professeur Andrew Pask, chef du laboratoire TIGRR, avec un fœtus de thylacine conservé et un spécimen de taxidermie. (Université de Melbourne)
Mais comment s’y prendre pour ressusciter une espèce éteinte ?
Dans le cas du mammouth laineux, le plan consiste à insérer des séquences d’ADN provenant d’échantillons de défenses, d’os et d’autres tissus de mammouth dans des cellules souches de son proche parent existant, l’éléphant d’Asie. Ce dernier ne diffère du mammouth laineux que par environ 1,4 million de bases d’ADN, ce qui correspond à plus de 1 600 gènes codant pour des protéines qui devraient être modifiés. Parmi ces gènes figurent ceux qui codent pour les poils denses et la graisse épaisse du mammouth, qui lui permettent de résister au froid, ainsi que pour son crâne haut bombé caractéristique.
Après avoir retiré l’ADN d’un ovule d’éléphant et l’avoir remplacé par l’ADN modifié de mammouths laineux à l’aide de l’édition génétique CRISPR, l’étape suivante consisterait à implanter l’embryon dans un utérus artificiel tapissé de tissu utérin cultivé à partir de cellules souches. Si tout se passe comme prévu, l’utérus artificiel sera le lieu de gestation d’une sorte d’hybride mammouth laineux-éléphant de 90 kg pendant deux ans. L’animal résultant serait mi-éléphant, mi-mammouth. Au final, ces hybrides seraient relâchés dans la nature, dans la toundra arctique en train de fondre, où des troupeaux de quasi-mammouths aideraient à abattre les arbres et la végétation qui absorbent la lumière du soleil, favorisant ainsi les prairies qui contribueraient à maintenir le sol plus froid et à protéger le pergélisol contre la fonte et la libération de méthane, un gaz à effet de serre très puissant. L’objectif est de réaliser tout cela d’ici 2027.
C’est très ambitieux et beaucoup de choses peuvent et vont probablement mal tourner. Mais ressusciter le thylacine semble plus facile. Le tigre de Tasmanie n’a disparu que depuis une centaine d’années, alors que 10 000 ans se sont écoulés depuis la mort du dernier mammouth laineux, échoué sur l’île de Wrangler, dans l’océan Arctique. Il est donc beaucoup plus facile d’extraire de l’ADN viable du thylacine que du mammouth laineux, dont le code génétique est dégradé et sujet à toutes sortes d’erreurs.
Ce n’est pas la première fois que l’on tente de ressusciter le tigre de Tasmanie. En 1999, des scientifiques australiens ont voulu cloner l’animal disparu en utilisant l’ADN extrait de spécimens conservés au musée australien. Cependant, le projet a été abandonné quelques années plus tard après qu’il soit devenu évident que la qualité de l’ADN était inexploitable.
Beaucoup de choses ont changé depuis lors. Les scientifiques disposent d’outils beaucoup plus avancés, tels que des appareils de séquençage génétique plus sophistiqués et plus fiables, le système CRISPR pour couper et coller les nucléotides (les éléments de base de l’ADN), et des algorithmes d’apprentissage automatique capables d’identifier les régions du génome censées remplir des fonctions particulières.
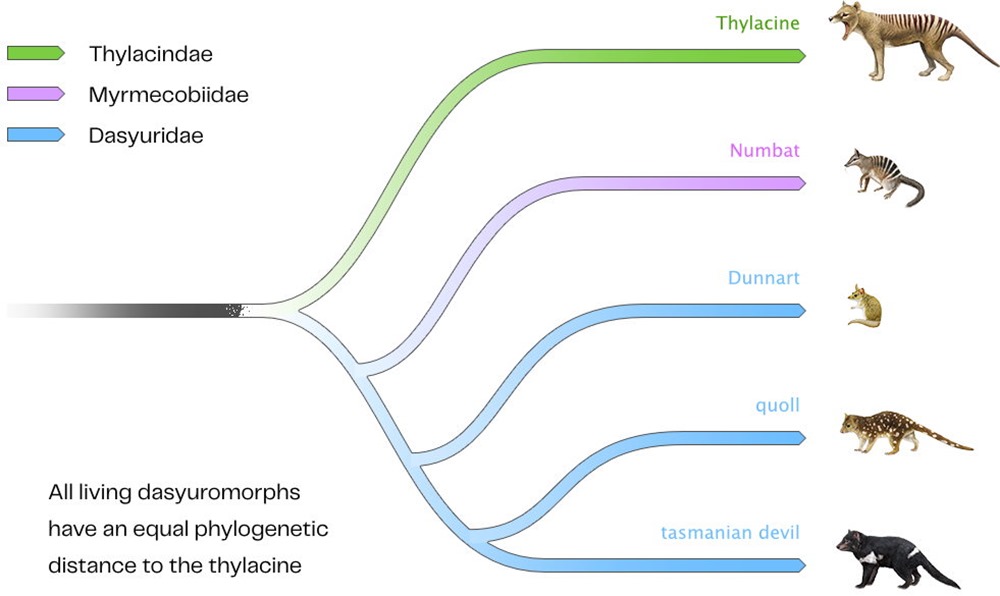
Mais cela restera un défi de taille. Tout comme le mammouth laineux a besoin de cellules d’éléphant comme échafaudage, Colossal prévoit de prélever des cellules sur le plus proche parent vivant du thylacine, un marsupial ressemblant à une souris, connu sous le nom de dunnart à pieds étroits(Sminthopsis crassicaudata). À l’aide d’outils d’IA sophistiqués, les scientifiques identifieraient toutes les régions où l’ADN du dunnart et celui du thylacine diffèrent l’un de l’autre. Il s’agit ensuite de remplacer les gènes du dunnart et d’insérer à leur place des séquences de thylacine à l’aide de CRISPR, afin de construire une cellule de thylacine et, finalement, un embryon de thylacine.
Un arbre phylogénétique montrant la relation entre le thylacine et les autres marsupiaux dasuridés. (Université de Melbourne)
L’embryon pourrait être cultivé dans la poche d’un marsupial de substitution, comme le dunnart, ou dans une chambre microfluidique qui imite artificiellement la poche du marsupial. Et comme pour le mammouth laineux, l’objectif est de réintroduire dans la nature ces hybrides de thylacine, qui pourraient contribuer à ramener les écosystèmes à un état antérieur, moins perturbé. Des dizaines de ces animaux devraient être élevés pour que ce “réensauvagement” ait une chance de réussir.
Selon le Dr Pask :
C’est un moment historique pour la recherche sur les marsupiaux et nous sommes fiers de faire équipe avec Colossal pour faire de ce rêve une réalité. La technologie et les principaux enseignements tirés de ce projet influenceront également la prochaine génération d’efforts de conservation des marsupiaux. En outre, la réintroduction du thylacine dans le paysage de Tasmanie peut considérablement freiner la destruction de cet habitat naturel par les espèces envahissantes. Le tigre de Tasmanie est une icône de la culture australienne. Nous sommes ravis de faire partie de cette équipe pour ramener cette espèce unique et fondamentale que l’humanité avait éradiquée de la planète.
Si ni le mammouth laineux ni le thylacine ne sont ressuscités, Colossal affirme que tout leur travail ne sera pas vain. Les technologies sur lesquelles ils travaillent actuellement pourraient être utilisées pour conserver les espèces actuellement vivantes qui sont au bord de l’extinction, et permettre de mieux comprendre les changements dans l’évolution d’innombrables espèces essentielles. Par exemple, ces progrès pourraient contribuer à doter d’autres espèces de gènes leur permettant de résister à des agents pathogènes ou de mieux supporter la chaleur et la sécheresse engendrées par le changement climatique.
On pourrait arguer que les dizaines de millions de dollars injectés dans ces projets sont gaspillés alors qu’ils pourraient servir à financer des mesures de conservation plus terre à terre. C’est certainement un point valable. Après tout, il vaut mieux prévenir que guérir. Lorsqu’on repousse les limites de la science, on court toujours le risque de se retrouver dans une impasse qui ne mène nulle part. Mais les récompenses peuvent en valoir la peine.
Le projet présenté sur le site de l’Université de Melbourne : Lab takes ‘giant leap’ toward thylacine de-extinction with Colossal genetic engineering technology partnership et la société Colossal.