Une bactérie génétiquement modifiée pour être immunisée contre tous les virus
Des chercheurs ont réalisé des progrès stupéfiants dans le domaine du génie génétique et de la biologie synthétique en modifiant une souche de la bactérie Escherichia coli afin de l’immuniser contre pratiquement toutes les infections virales.
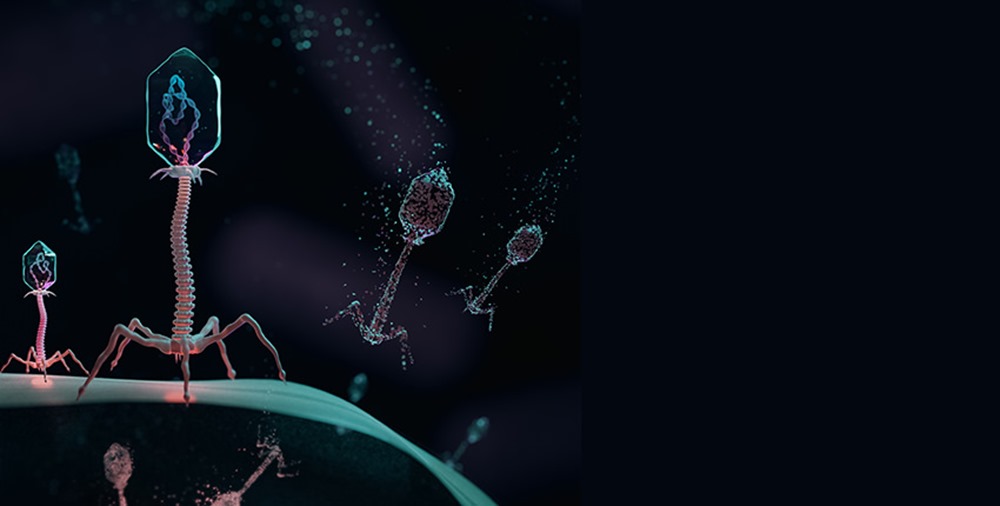
Image d’entête : illustration de virus appelés phages infectant une cellule de bactérie. (Behnoush Hajian/ Harvard Medical School)
Bien que les chercheurs ne puissent pas garantir qu’aucun virus ne puisse jamais infecter cette souche modifiée d’E. coli, aucun des nombreux types de virus qu’ils ont essayés n’a été capable d’atteindre la bactérie.
Cette technologie pourrait réduire la menace de contamination virale lors de l’utilisation de bactéries comme bio-usine pour produire des substances utiles telles que l’insuline et les biocarburants. Dans les grandes cuves de bactéries, les infections virales peuvent interrompre la production, compromettre la qualité des médicaments et entraîner d’importants coûts.
Bien qu’une bactérie exempte de virus qui s’échappe dans la nature constitue un risque biologique inquiétant, les scientifiques ont pris un certain nombre de mesures pour protéger leur organisme génétiquement modifié et prévenir tout incident indésirable.
Le premier auteur de l’étude, Akos Nyerges, chercheur en génétique dans le laboratoire de George Church à l’Institut Blavatnik de la Harvard Medical School et à l’Institut Wyss pour l’ingénierie inspirée par la biologie (États-Unis), affirme que l’équipe a mis au point la première technologie capable de concevoir un organisme immunisé contre tout virus connu.
Nyerges affirme que, bien qu’elle ne puisse pas prétendre que la bactérie soit totalement résistante aux virus, l’équipe n’a pas trouvé, sur la base d’expériences de laboratoire et d’analyses informatiques approfondies, de virus capable d’en venir à bout.
Les travaux des chercheurs s’inscrivent dans le prolongement des précédentes tentatives des ingénieurs généticiens de produire des bactéries résistantes aux virus. En 2022, un groupe de l’université de Cambridge pensait avoir créé une souche d’E. coli immunisée contre les virus. Toutefois, lorsque Nyerges et ses collègues ont mis cette affirmation à l’épreuve, ils ont été déçus de constater que les virus pouvaient facilement infecter les bactéries modifiées.
L’équipe a prélevé des échantillons dans divers environnements, notamment des poulaillers, des nids de rats, des eaux usées et la rivière Muddy, située près du campus de la Harvard Medical School. Les méchants virus qu’ils ont isolés étaient capables d’infecter les bactéries modifiées.
La méthode de Cambridge pour empêcher les virus d’infecter l’E. coli consistait à réduire le nombre de codons de cette bactérie à 61, contre 64 à l’état naturel. Un codon est une séquence d’ADN ou d’ARN de trois nucléotides (un trinucléotide) qui forme une unité d’information génomique codant pour un acide aminé particulier ou signalant la fin de la synthèse des protéines.
Sans les codons manquants, un virus ne devrait pas pouvoir détourner les cellules d’un organisme. C’est une idée assez brillante, mais elle n’est pas parfaite. Il manquait quelque chose qui permettait encore à certains virus d’infecter les cellules.
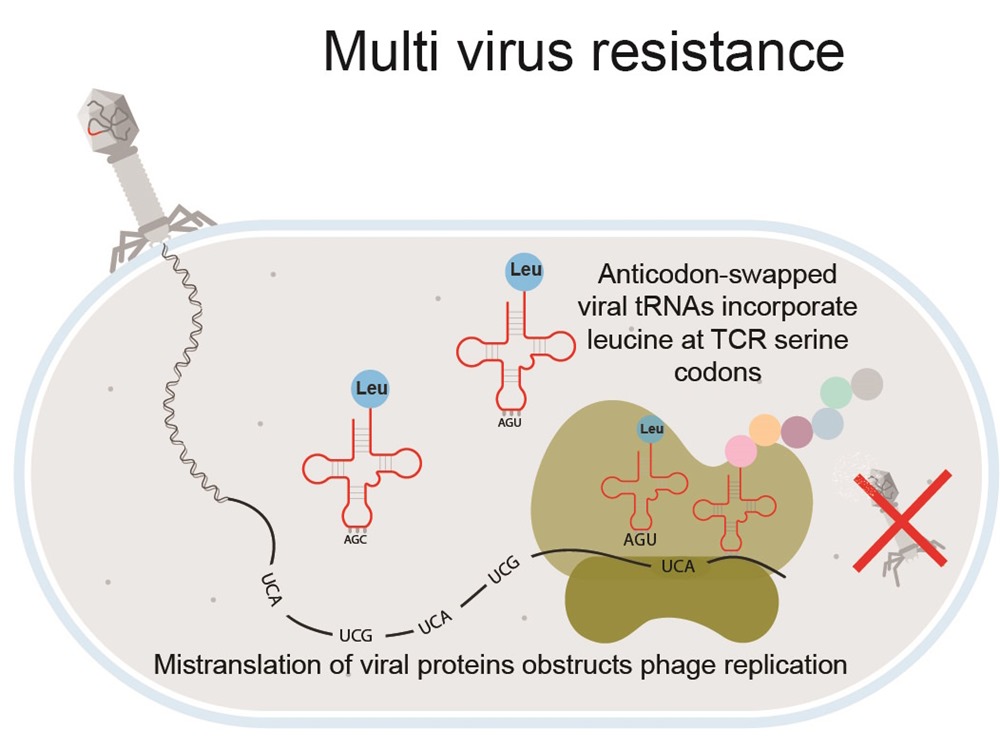
En plus de supprimer des codons, les chercheurs de Harvard ont ajouté un type spécifique d’ARN appelé acides ribonucléiques de transfert, abrégé ARNt. Cette molécule d’ARN reconnaît un codon spécifique et ajoute ensuite des acides aminés à la protéine qui doit être produite. Par exemple, le codon TCG indique à l’ARNt qui lui correspond qu’il doit ajouter l’acide aminé sérine.
Lorsque l’équipe de Cambridge a supprimé le TCG, elle a également supprimé les ARNt correspondants. Mais au lieu de les supprimer, les chercheurs de Harvard ont ajouté des ARNt “trompeurs” qui introduisent des acides aminés différents de ceux qu’ils devraient. Par exemple, lorsque l’ARNt modifié voit le TCG, il ajoute de la leucine au lieu de la sérine.
Selon Nyerges :
La leucine est à peu près aussi différente de la sérine qu’il est possible de l’être, physiquement et chimiquement.
Lorsque les virus ont essayé de signaler aux bactéries E. coli de produire des protéines virales, les ARNt trompeurs ont ajouté les mauvais acides aminés, ce qui a donné lieu à des protéines virales mal repliées et non fonctionnelles. Le virus ne pouvait plus se répliquer et infecter d’autres cellules.
A partir de l’étude : représentation d’une bactérie Escherichia coli immunisée, subissant l’attaque d’un virus phage (en gris haut à gauche) qui introduit ses protéines virales. (A. Nyerges et col./ Nature)
Bien que les virus soient dotés de leurs propres ARNt capables de transformer le TCG en sérine, les chercheurs ont constaté que les ARNt trompeurs qu’ils ont introduits étaient si efficaces qu’ils l’emportaient sur leurs homologues viraux.
En théorie, un virus pourrait éventuellement muter pour surmonter les codons et les ARNt échangés. Toutefois, Nyerges ajoute qu’il faudrait des dizaines de mutations très spécifiques en même temps pour permettre au virus de passer par la “porte arrière”.
C’est très, très improbable pour l’évolution naturelle.
La technologie comprend deux mesures de protection majeures afin d’éviter que ces organismes modifiés ne se répandent dans la nature. La première mesure vise à offrir une protection contre le transfert horizontal de gènes, qui se produit lorsque des fragments de code génétique et leurs caractéristiques correspondantes, telles que la résistance aux antibiotiques, sont transférés d’un organisme à l’autre. Ce transfert se distingue du transfert vertical, dans lequel le matériel génétique est transmis d’un parent à sa progéniture après qu’ils ont eu des rapports sexuels ou qu’ils se sont clonés. Il n’est pas rare de voir des bactéries partager des gènes avec des animaux et même des plantes.
Lorsqu’un autre organisme rencontre l’E. coli modifié et partage les ARNt trompeurs, l’interprétation erronée des codons sérine endommage ou tue la cellule réceptrice, empêchant ainsi la propagation.
Toujours selon Nyerges :
Les ARNt modifiés qui s’échappent ne vont pas loin, car ils sont toxiques pour les organismes naturels.
La seconde sécurité empêche les bactéries elles-mêmes de croître et de proliférer en dehors d’un environnement contrôlé. L’E. coli modifié dépend à 100 % d’acides aminés fabriqués en laboratoire et impossibles à trouver dans la nature. Si les bactéries devaient sortir du laboratoire ou de la bio-usine et s’échapper, elles mourraient de faim.
Les auteurs ont déclaré que leur technique pourrait avoir d’importantes implications pour les stratégies de confinement biologique et le développement des OGM. Les virus n’étant plus un problème, les chercheurs pourraient utiliser des bactéries modifiées pour produire des substances biologiques précieuses, telles que des biocarburants ou de l’insuline, sans risque de contamination virale. En outre, cette technique pourrait ouvrir la voie au déploiement en toute sécurité de cultures génétiquement modifiées, réduisant ainsi la propagation des maladies et renforçant potentiellement la sécurité alimentaire.
Toutefois, certains experts soulignent que l’utilisation d’organismes génétiquement modifiés, même s’ils sont dotés de mesures de sécurité intégrées, soulève encore des problèmes éthiques et environnementaux.
Malgré ces inquiétudes, la percée de l’équipe de la Harvard Medical School représente une avancée significative dans le domaine du génie génétique et de la biologie synthétique. En créant une bactérie immunisée contre tous les virus connus, ils ont ouvert de nouvelles possibilités d’exploiter la puissance des bactéries pour produire des substances utiles, tout en minimisant le risque de contamination et de flux génétique.
Nous disposons désormais d’un modèle permettant d’immuniser n’importe quel organisme contre les virus et d’empêcher les flux de gènes à l’intérieur et à l’extérieur des OGM, ce qui ouvre la voie à des stratégies de confinement biologique plus sûres et plus efficaces à l’avenir.
L’étude publiée dans Nature : A swapped genetic code prevents viral infections and gene transfer et présentée sur le site de la Harvard Medical School : Designing More Useful Bacteria.