D’anciens virus à l’origine de l’évolution des cerveaux complexes
Selon une nouvelle étude, des rétrovirus pourraient avoir déclenché l’évolution vers des cerveaux larges et complexes chez les vertébrés il y a des centaines de millions d’années.
Image d’entête : particules du virus VIH-1, un exemple de rétrovirus. (NIAID/ Flickr)
En approfondissant nos connaissances sur l’évolution du cerveau chez les vertébrés, nous pourrions comprendre comment celui des humains est devenu si grand et si complexe.
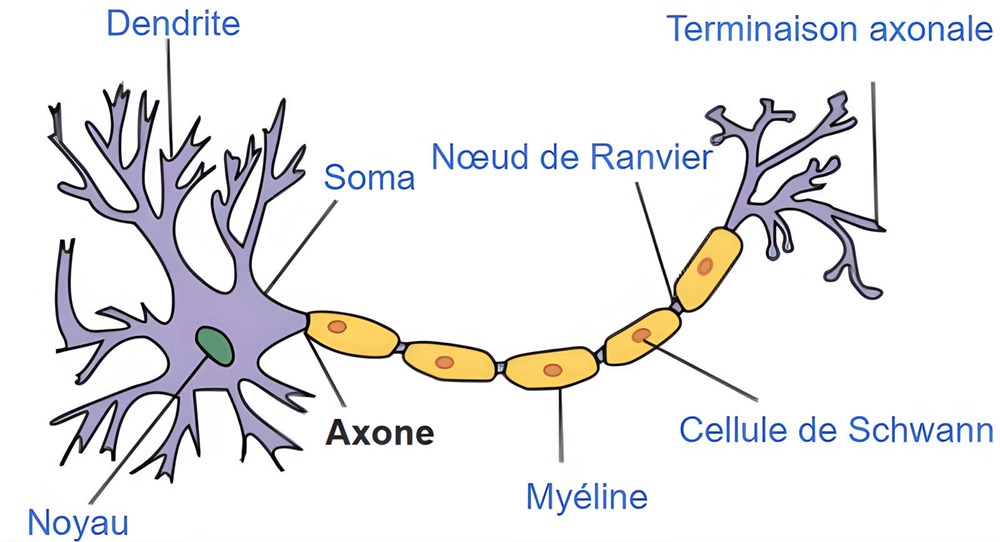
Un élément génétique rétroviral, appelé « rétrotransposon« , pourrait être à l’origine de la production de myéline par les mammifères, les amphibiens, les reptiles, les oiseaux et les poissons, laquelle est constituée de protéines et de substances grasses. La myéline est une couche isolante qui protège l’axone des cellules nerveuses, comme le montre le schéma ci-dessous. Cette « gaine » permet d’accélérer la transmission des signaux électriques entre les neurones. L’utilisation de la myéline a permis d’accélérer la transmission des signaux sans augmenter le diamètre de l’axone. Cela signifie que le cerveau des vertébrés peut contenir plus de neurones.
Structure typique d’un neurone. (Wikimedia)
La séquence génétique, appelée « RetroMyelin« , est décrite dans une étude publiée la semaine dernière (lien plus bas).
Selon le coauteur de l’étude, Robin Franklin, neuroscientifique d’Altos Labs-Cambridge Institute of Science (Etats-Unis) :
Les rétrovirus ont été nécessaires pour que l’évolution des vertébrés prenne son essor. Si les rétrovirus n’avaient pas inséré leurs séquences dans le génome des vertébrés, la myélinisation n’aurait pas eu lieu, et sans myélinisation, toute la diversité des vertébrés telle que nous la connaissons n’aurait jamais vu le jour.
La myéline est apparue à peu près au même moment que le développement des mâchoires chez d’anciens poissons. Les premiers poissons à mâchoires, comme le Bothriolepis canadensis, vieux de 380 millions d’années, représenté ci-dessous, ont entraîné une révolution dans l’évolution. Ces nouvelles mâchoires ont coïncidé avec le développement des membres qui allaient permettre aux vertébrés de quitter les anciens océans, et avec l’évolution des grands cerveaux chez les animaux à colonne vertébrale, pourraient y être intimement liées.
Reconstitution vivante du Bothriolepis canadensis. (Nobu Tamura/ Wikimedia)
Selon Franklin :
L’évolution a poussé nos axones à accélérer la conduction des impulsions, car une conduction plus rapide permet d’attraper ou de fuir les choses plus rapidement.
L’importance de la myéline dans l’évolution des vertébrés est connue depuis longtemps. Mais la façon dont elle est apparue pour la première fois est restée, jusqu’à présent, un mystère. Les chercheurs se sont penchés sur cette question en étudiant les réseaux de gènes dans les oligodendrocytes, les cellules qui produisent la myéline dans le système nerveux central.
Selon le premier auteur, Tanay Ghosh, biologiste informatique travaillant également à Altos Labs-Cambridge Institute of Science :
Les rétrotransposons composent environ 40 % de nos génomes, mais on ne sait pas comment ils ont pu aider les animaux à acquérir des caractéristiques spécifiques au cours de l’évolution. Notre motivation était de savoir comment ces molécules contribuent aux processus évolutifs, en particulier dans le contexte de la myélinisation.
L’inhibition de RetroMyelin chez les rongeurs a montré que la production de myéline s’arrêtait. Des séquences similaires ont été trouvées chez d’autres vertébrés à mâchoire, mais pas chez les vertébrés sans mâchoire ni chez les invertébrés.
En construisant un arbre phylogénétique de 22 espèces de vertébrés à mâchoires, les chercheurs ont pu comparer les séquences de RetroMyelin. Cette comparaison a révélé des différences entre les espèces, ce qui suggère que la RetroMyelin a été incorporée dans le génome à plusieurs reprises au cours de l’évolution des vertébrés à mâchoires.
L’étude publiée dans Cell : A retroviral link to vertebrate myelination through retrotransposon-RNA-mediated control of myelin gene expression.