Comment les ovules humains restent-ils en sommeil et aptes à la reproduction pendant des décennies dans les ovaires ?
Les ovocytes humains, dont certains se transformeront en ovules, se forment avant la naissance et peuvent rester viables sur le plan reproductif jusqu’à 50 ans avant d’être fécondés. Mais comment peuvent-ils rester en sommeil et en bonne santé dans les ovaires pendant si longtemps ?
Selon une nouvelle étude, la réponse réside dans leur activité métabolique altérée, c’est-à-dire l’absence d’utilisation d’un complexe protéique et enzymatique clé (complexe respiratoire I).
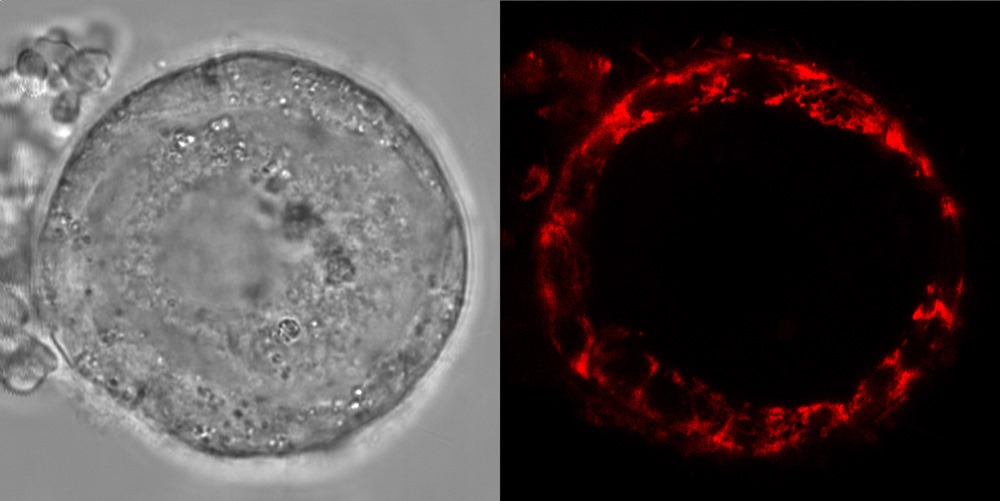
Image d’entête, à partir de l’étude : Imagerie cellulaire en temps réel d’un follicule humain, montrant les cellules de la granulosa sur la couche externe, qui soutiennent l’ovocyte, contenu à l’intérieur. L’activité des espèces réactives de l’oxygène (ERO) est indiquée en rouge. (Aida Rodriguez et col./ Nature)
Pour générer de l’énergie dans leur état de dormance et éviter de créer des molécules nocives susceptibles d’endommager l’ADN et de provoquer la mort cellulaire, les ovules humains utilisent des voies métaboliques alternatives jamais observées auparavant dans d’autres types de cellules animales.
Selon l’auteure principale, Aida Rodriguez-Nuevo, chercheuse postdoctoral au Centre de régulation génomique (CRG), en Espagne :
Les humains naissent avec toute la réserve d’ovules dont ils disposeront au cours de leur vie. Comme l’humain est aussi le mammifère terrestre qui vit le plus longtemps, les ovules doivent conserver un état vierge tout en évitant des décennies d’usure.
Nous montrons que ce problème est résolu en contournant une réaction métabolique fondamentale qui est aussi la principale source de dommages pour la cellule. En tant que stratégie de maintenance à long terme, c’est comme mettre les batteries en mode veille.
Cela représente un tout nouveau paradigme jamais vu auparavant dans les cellules animales.
Les ovules humains se forment d’abord dans les ovaires au cours du développement fœtal. Au cours des premiers stades de la maturation, les ovules immatures (appelés ovocytes) sont mis en arrêt cellulaire et peuvent rester dormants pendant des décennies.
Pendant cette période, les mitochondries de l’ovocyte, qui sont en quelque sorte les batteries de la cellule, produisent juste assez d’énergie pour répondre aux besoins de la cellule.
Pour savoir comment elles y parviennent, les chercheurs ont utilisé une combinaison de techniques d’imagerie en direct, de protéomique (étude à grande échelle des protéines) et de biochimie pour étudier cette production d’énergie dans des ovocytes humains et de Xenopus (grenouille aquatique).
Il est intéressant de noter que les ovocytes n’utilisent pas une protéine de base, appelée complexe I, qui déclenche les réactions générant de l’énergie dans les mitochondries de la plupart des autres cellules.
En fait, le complexe I est pratiquement absent des ovocytes. Cela leur permet d’éviter de créer des molécules connues sous le nom d’espèces réactives de l’oxygène (ERO), des molécules contenant de l’oxygène qui réagissent facilement avec d’autres produits chimiques. Les ERO sont des sous-produits normaux du métabolisme cellulaire, mais ils sont nocifs lorsqu’ils s’accumulent, endommageant la fonction normale de l’ADN, des protéines et d’autres composants cellulaires, et provoquant finalement la mort cellulaire.
Ils sont également associés à des taux plus faibles de fécondation et de survie des embryons.
L’imagerie en direct a montré que ni les ovocytes précoces de Xenopus ni ceux de l’humain ne présentaient de signal ERO détectable.
Selon les auteurs de l’étude, cette découverte explique pourquoi certaines personnes atteintes d’affections mitochondriales liées au complexe I ne connaissent pas de baisse de fertilité, par rapport aux personnes atteintes d’affections touchant d’autres complexes respiratoires mitochondriaux.
Cette découverte pourrait également déboucher sur de nouvelles stratégies pour aider à préserver les réserves d’ovules humains des patients soumis à un traitement contre le cancer.
Selob l’auteur principal, le Dr Elvan Böke, chef de groupe du programme de biologie cellulaire et développementale du CRG :
Les inhibiteurs du complexe I ont déjà été proposés comme traitement du cancer. Si ces inhibiteurs s’avèrent prometteurs dans de futures études, ils pourraient potentiellement cibler les cellules cancéreuses tout en épargnant les ovocytes.
L’équipe prévoit de poursuivre ces recherches afin de découvrir la source d’énergie exacte que les ovocytes humains utilisent à la place du complexe I.
Böke de conclure :
Un cas d’infertilité féminine sur quatre est inexpliqué, ce qui indique une énorme lacune dans notre compréhension de la reproduction féminine. Notre ambition est de découvrir les stratégies (telles que l’absence de complexe I) que les ovocytes emploient pour se maintenir en bonne santé pendant de nombreuses années, afin de comprendre pourquoi ces stratégies finissent par échouer avec l’âge avancé.
L’étude publiée dans Nature : Oocytes maintain ROS-free mitochondrial metabolism by suppressing complex I et présentée sur le site du Centre for Genomic Regulation (CRG) : Human eggs remain healthy for decades by putting ‘batteries on standby mode’.