Des scientifiques déclarent avoir produit des structures semblables à celles d’un embryon à partir de cellules souches de singe
Des scientifiques ont, pour la première fois, cultivé des modèles embryonnaires à partir de cellules souches de singe, qui, implantées dans des « mères » porteuses, semblent progresser jusqu’aux premiers stades de la gestation.
Des versions humaines de ces modèles ont déjà été créées à partir de cellules souches (lien ci-dessous), mais jusqu’à récemment, une limite de 14 jours s’appliquait aux scientifiques qui les cultivaient à des fins de recherche. De plus, il est actuellement hors de question de les transplanter dans une mère porteuse humaine, ce qui rend difficile l’utilisation de ces modèles pour étudier le développement embryonnaire dans des conditions réelles.
Précédemment, en 2021 :
À la recherche d’une autre approche, une équipe de chercheurs chinois s’est tournée vers l’espèce la plus proche possible : le macaque crabier (Macaca fascicularis).
Les scientifiques ont exposé des cellules souches embryonnaires de macaque, dans une culture cellulaire, à une sélection minutieuse de facteurs de croissance. Les cellules ont ensuite formé des structures ressemblant à des embryons, appelées “blastoïdes” (terme qui distingue ces structures dérivées de cellules souches des blastocystes naturels).
Un quart des cellules souches de l’expérience ont évolué vers une forme blastoïde, un taux de réussite comparable à celui d’expériences précédentes utilisant des cellules souches embryonnaires humaines. Ces cellules ont ensuite été cultivées en laboratoire jusqu’à ce qu’elles commencent à former trois couches distinctes dans le cadre d’un processus connu sous le nom de gastrulation, un moment clé du développement embryonnaire qui met en place un plan corporel de base. Plusieurs de ces blastoïdes ont progressé pour former une vésicule vitelline et un amnios (la membrane remplie de liquide qui recouvre l’embryon en développement).
Au microscope, les scientifiques ont remarqué que les blastoïdes présentaient des caractéristiques similaires à celles des embryons de stade 7 (chez les humains, ce stade survient environ 18 à 21 jours après la fécondation). Ce modèle d’embryon de singe a eu tendance à s’effondrer à environ 18 jours de croissance en dehors d’un corps, bien que les chercheurs prévoient d’explorer dans de futures expériences d’autres systèmes qui ont réussi à cultiver des blastoïdes de souris. La création des blastoïdes de singe ne représentait que la moitié de l’expérience : certains ont également été transplantés dans l’utérus de huit singes femelles.
Les scientifiques ont sélectionné des blastoïdes qui avaient été cultivés pendant sept jours, qui présentaient une masse cellulaire interne et externe et une cavité visible, car ce sont des caractéristiques essentielles aux embryons naturels. Chaque singe de substitution a été « imprégné » de 8 à 10 blastoïdes et surveillé à l’aide d’ultrasons et de tests hormonaux au cours des 20 jours suivants.
Les structures ressemblant à des embryons se sont implantées dans trois des mères porteuses, formant des sacs de gestation précoce (la membrane remplie de liquide qui renferme l’embryon et le liquide amniotique) qui ont duré une semaine ou plus après la transplantation. Les mères porteuses présentaient également des taux accrus de progestérone et de gonadotrophine chorionique, hormones associées à la grossesse.
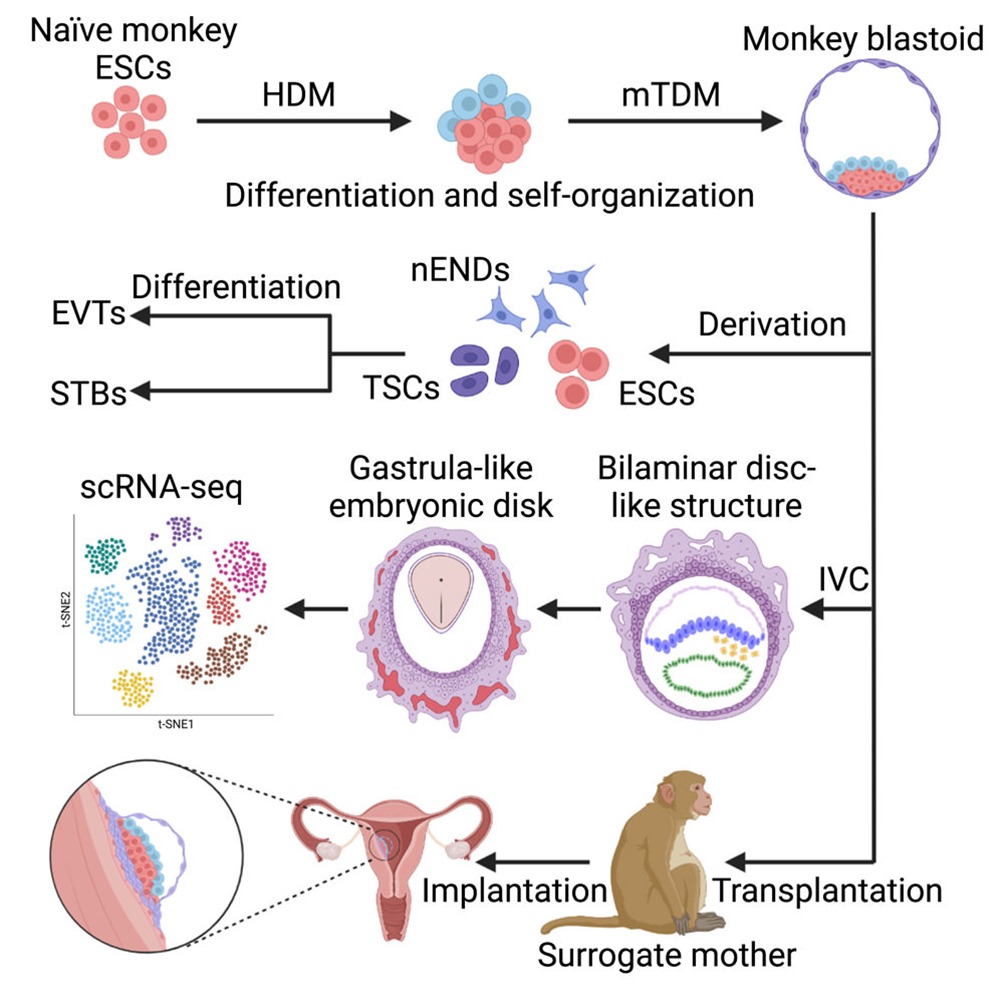
Résumé graphique de l’étude : Un modèle d’embryon de singe cynomolgus présente une gastrulation et un début de grossesse. (Li et col./ Cell Stem Cell)
Toutes les structures embryonnaires avaient entièrement disparu au bout d’une semaine environ, mais le fait qu’elles se soient implantées et qu’elles aient déclenché la libération de ces hormones suggère que, pendant un bref instant, les singes étaient en fait enceintes.
La réalisation d’expériences similaires à l’aide de cellules humaines et de mères porteuses pourrait nous en apprendre beaucoup sur notre propre biologie et sur son potentiel à engendrer des maladies, mais à un coût éthique que peu de personnes seraient prêtes à payer. L’utilisation de macaques s’accompagne de sa propre controverse : les expériences sur les primates de ce type sont interdites dans de nombreux endroits du monde.
L’un des coauteurs de l’étude, le neuroscientifique Qiang Sun, est directeur du centre de recherche sur les primates non humains de l’Académie chinoise des sciences (CAS), où l’expérience a été menée. Au cours de sa carrière, il a créé une paire de macaques clonés, Zhong Zhong et Hua Hua, et il a découvert un raccourci vers la maturité sexuelle en greffant le tissu testiculaire de jeunes macaques sur des souris.
Selon Qiang Sun :
La production rapide et efficace d’un grand nombre de modèles de singes génétiquement modifiés favorisera le développement de modèles animaux pertinents pour les troubles humains et approfondira notre compréhension des mécanismes dans le domaine des sciences de la vie.
D’autres estiment que de telles expériences ne se justifient pas, car les études animales ne permettent pas de prédire de manière fiable les résultats chez l’humain et se traduisent rarement par des traitements concrets.
Zhen Liu, scientifique spécialiste de la reproduction et coauteur de l’étude, a déclaré que l’expérience aiderait à comprendre l’embryogenèse humaine, car les singes sont très proches de l’humain.
Zhen Liu ajoute :
Nous espérons que l’étude de ces modèles permettra d’approfondir notre compréhension du développement embryonnaire humain, et notamment de mettre en lumière certaines des causes des fausses couches précoces.
L’étude publiée dans Cell Stem Cell : Cynomolgus monkey embryo model captures gastrulation and early pregnancy.