Des scientifiques ont enfin cartographié l’ensemble du génome humain
Au cours des deux dernières décennies, des centaines de scientifiques du monde entier affiliés au projet génome humain, dont le coût s’élève à 3 milliards de dollars, ont cherché à lire chaque lettre du code génétique d’une personne. En 2003, la première carte du génome humain a été publiée, une percée capitale qui a marqué le début d’une nouvelle ère scientifique. Mais il ne s’agissait pas d’une carte complète. Il manquait environ 8 % du génome, soit l’équivalent des informations contenues dans un chromosome. Cette région délicate du génome contenait des séquences hautement répétitives qui étaient difficiles à reconstituer, jusqu’à présent.
Selon Eric Green, directeur du National Human Genome Research Institute (NHGRI), qui fait partie des Instituts américains de la santé :
La production d’une séquence du génome humain véritablement complète représente une incroyable réussite scientifique, car elle offre la première vue d’ensemble de notre empreinte génétique. Cette information fondamentale renforcera les nombreux travaux en cours visant à comprendre toutes les nuances fonctionnelles du génome humain, ce qui, à son tour, renforcera les études génétiques des maladies humaines.
Le génome est la somme de toutes les séquences d’ADN et d’ADN mitochondrial (ADNmt) de la cellule. Il contient toutes les instructions dont un être vivant a besoin pour survivre et se répliquer. Il est constitué de blocs de construction chimiques ou « bases azotées » (G, A, T et C), dont l’ordre ou la séquence code l’information biologique.
Pour l’humain, la taille du génome est considérée comme étant le nombre total de bases dans une copie de son ADN nucléaire. Et ce, malgré le fait que les humains et les autres mammifères contiennent des copies doubles de presque tout leur ADN. Par exemple, nous avons des paires de chromosomes, un chromosome de chaque paire étant hérité de chaque parent. Mais les scientifiques ne s’intéressent qu’au séquençage de la somme des bases d’une copie de chaque paire de chromosomes. Le génome réel d’une personne fait environ six milliards de bases, mais une seule copie « représentative » du génome humain fait environ trois milliards de bases.
Comme il est très grand, il est pratiquement impossible de le lire en une seule fois, de la tête aux pieds. Pour séquencer le génome, les chercheurs commencent par décomposer l’ADN en morceaux plus petits et plus faciles à gérer. Chaque chaîne est ensuite soumise à des réactions chimiques qui permettent aux scientifiques de repérer l’emplacement des bases et leur position respective dans la séquence. Il ne reste plus qu’à assembler ces morceaux comme on résout un puzzle géant.
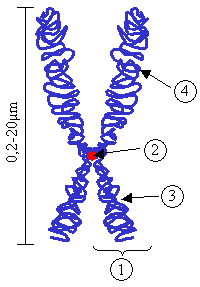 Le problème est que certaines régions du génome, en particulier les centromères (les parties qui maintiennent les deux brins de chromosomes ensemble, 2 dans l’image ci-contre), répètent les mêmes séquences encore et encore. Dans le passé, ces régions répétitives rendaient pratiquement impossible l’assemblage du génome dans le bon ordre, comme s’il s’agissait d’un puzzle complexe composé de nombreuses pièces identiques. Pour ajouter au défi, le génome contient deux copies , l’une de la mère, l’autre du père, et il est facile de combiner leurs séquences.
Le problème est que certaines régions du génome, en particulier les centromères (les parties qui maintiennent les deux brins de chromosomes ensemble, 2 dans l’image ci-contre), répètent les mêmes séquences encore et encore. Dans le passé, ces régions répétitives rendaient pratiquement impossible l’assemblage du génome dans le bon ordre, comme s’il s’agissait d’un puzzle complexe composé de nombreuses pièces identiques. Pour ajouter au défi, le génome contient deux copies , l’une de la mère, l’autre du père, et il est facile de combiner leurs séquences.
Image ci-contre : représentation d’un chromosome. (1) Chromatide. Chacune formée d’un brin d’ADN parental et d’un brin d’ADN néoformé obtenu après réplication durant la phase S ; (2) Centromère. Le point de contact des deux chromatides, et le point de séparation lors de la mitose ; (3) Bras court ; (4) Bras long. (Magnus Manske/ Wikimedia)
Au départ, ce problème n’était pas considéré comme très important. On considérait les séquences répétitives de l’ADN comme des « déchets« , c’est-à-dire des copies supplémentaires n’ayant que peu ou pas d’importance dans le contexte général. Il s’est avéré par la suite que c’était une erreur de jugement. Les centromères contiennent des instructions vitales pour la fabrication des protéines, tandis que d’autres sections répétitives peuvent contenir des gènes uniques qui ont aidé notre espèce à s’adapter au cours de son évolution.
Comme les centromères jouent un rôle essentiel dans la copie précise du matériel génétique, lorsqu’une cellule se divise en deux, des dysfonctionnements peuvent entraîner des maladies telles que la trisomie 21, une maladie héréditaire dans laquelle les enfants naissent avec un chromosome supplémentaire.
Ces difficultés ont été surmontées grâce à la technologie moderne et à une réflexion très intelligente. À l’université de Pittsburgh (États-Unis), les généticiens de la reproduction conservent des échantillons de cellules humaines très rares qui, en raison de problèmes de développement, comportent deux copies de l’ADN du père et aucune information de la mère. Cette lignée à génome unique est beaucoup plus facile à séquencer que le génome typique à deux copies dont nous héritons tous.
Cet échantillon de lignée “monogénome” a été analysé à l’aide d’un nouveau Nanopore qui peut lire un million de lettres d’ADN à la fois. Pendant qu’ils travaillaient sur ce projet, les chercheurs se sont regroupés pour former le consortium Telomere-to-Telomere (T2T) afin de séquencer chaque chromosome d’une extrémité, ou télomère, à l’autre.
Pendant 6 mois, les chercheurs du T2T ont séquencé le génome humain sans interruption. La dernière pièce du puzzle était une nouvelle machine de séquençage mise au point par la société américaine de biotechnologie Pacific Biosciences, capable d’effectuer un séquençage à lecture longue avec une précision supérieure à 99 %.
Selon Adam Phillippy, de l’Institut national de recherche sur le génome humain, qui a dirigé l’équipe de plus de 100 scientifiques ayant participé à cette recherche :
C’était la dernière pièce du puzzle, comme si on mettait une nouvelle paire de lunettes.
Globalement, la version complète du génome humain, désormais complète, contient 3,055 milliards de paires de bases, correspondant à 19 969 gènes. Parmi ces gènes, environ 2 000 sont nouveaux pour la science. Cependant, la plupart sont désactivés, ce qui signifie qu’ils n’expriment pas de protéines, et seuls 115 sont actifs. Les chercheurs ont également découvert des niveaux élevés et inattendus de variations génétiques dans les centromères, dont la signification reste à déterminer.
Les auteurs de l’étude ont décrit l’achèvement de la séquence du génome humain comme la pose d’une nouvelle paire de lunettes : nous pouvons désormais tout voir clairement. À l’avenir, armés de ces informations génomiques complètes, les médecins seront en mesure de fournir des soins de santé personnalisés à leurs patients. La première séquence du génome humain a coûté des milliards. Aujourd’hui, cartographier le génome d’un patient, y compris les lacunes récemment comblées, ne coûtera pas plus de 1 000 dollars (900 eur environ).
Mais en définitive, il est essentiel de disposer d’un génome complet pour reconstituer le cours de l’évolution humaine. Certains des gènes précédemment associés à des cerveaux plus gros se sont révélés très variables. Une personne peut avoir 10 copies d’un gène particulier, tandis que d’autres n’en ont qu’une ou deux. Cette variation est une arme à double tranchant, car « ces régions deviennent un creuset pour les changements évolutifs rapides et la susceptibilité aux maladies, tant au sein des espèces qu’entre elles », explique Eichler.
Ce travail monumental est cependant loin d’être terminé. Le consortium T2T est occupé à séquencer un nouveau génome, cette fois avec des chromosomes différents hérités de chaque parent. Un autre objectif ambitieux est de réaliser une étude d’association pangénomique, dans lequel l’ADN de centaines de personnes à travers le monde est entièrement séquencé afin de saisir au mieux la richesse de la diversité humaine.
En 2021, les chercheurs avaient déjà publié une étude détaillant ces résultats sur le serveur de prépublications bioRxiv, mais ils ont maintenant été évalués par des pairs. Les nouveaux résultats ont donc été publiés dans la revue Science : The complete sequence of a human genome et dans plus d’une douzaine d’autres études disponible sur le site du consortium Telomere-to-Telomere et présentés sur le site du National Human Genome Research Institute : Researchers generate the first complete, gapless sequence of a human genome.


