Une mise à jour de la précision de l’outil d’édition génétique CRISPR permet de traiter pléthore de maladies génétiques
Des scientifiques américains ont mis au point un nouveau et puissant système d’édition du génome qui pourrait offrir beaucoup plus de précision et d’efficacité que la méthode actuelle d’édition génétique (“Copier/ coller”) CRISPR-Cas9.
Petit rappel : Il n’y a pas si longtemps, en 2013, la Femme (…) a mis au point une technique révolutionnaire de manipulation génétique, le CRISPR–Cas9. Elle permet, en gros, de couper / coller des séquences de gènes. La Cas9 est le couteau, une enzyme (endonucléase) spécialisée dans la découpe de séquence ADN et on l’utilise donc pour couper celle que l’on veut éditer. CRISPR est une famille de séquences d’ADN que l’on trouve dans les génomes d’organismes procaryotes comme les bactéries et les archées. L’enzyme Cas9 (ou « CRISPR-associated protein 9 ») utilise les séquences CRISPR comme guide pour reconnaître et cliver des brins spécifiques d’ADN qui sont complémentaires de la séquence CRISPR. Les enzymes Cas9 et les séquences CRISPR forment la base d’une technologie connue sous le nom de CRISPR-Cas9 qui peut être utilisée pour éditer les gènes dans les organismes. Ce processus d’édition a une grande variété d’applications incluant la recherche biologique fondamentale, le développement de produits biotechnologiques et le traitement des maladies.
Image d’entête : structure de l’enzyme d’édition de gènes Cas9 interagissant avec de l’ARN et de l’ADN. (Gabriel Velez/ Mahajan Lab)
Bien que CRISPR-Cas9 soit une technologie médicale révolutionnaire qui jette les bases modernes de l’édition du code génétique, y compris les variantes associées à une maladie, on s’inquiète depuis longtemps de sa potentielle imprécision. Plus précisément, beaucoup craignent que l’édition CRISPR-Cas9 n’introduise des erreurs sous la forme d’insertions et de suppressions non contrôlées (hors cible) dans le code génétique, appelées indels.
Selon les chercheurs, le nouveau système, que ses inventeurs du Broad Institute du Massachusetts Institute of Technology (MIT) et de l’Université Harvard ont surnommé « prime editing« , pourrait changer la donne grâce à une nouvelle protéine qui permet une édition de haute précision des cibles génétiques.
Selon David Liu, biologiste du génome au Broad Institute :
L’une des principales aspirations des sciences moléculaires de la vie est la capacité d’apporter des changements précis au génome dans n’importe quel endroit.
Nous ne sommes pas au courant d’une autre technologie d’édition dans les cellules de mammifères qui offre ce niveau de polyvalence et de précision avec si peu de sous-produits.
La base de la nouvelle méthode d’édition prime editing est une enzyme appelée transcriptase inverse. Le système CRISPR utilise également une enzyme, Cas9, pour couper des brins d’ADN afin d’insérer un code génétique alternatif.
Une percée réalisée en 2017 par le laboratoire de Liu a grandement amélioré la précision du système, permettant des changements d’une seule lettre dans les paires de bases d’ADN au lieu de remplacer des portions entières de code à la fois.
Maintenant, grâce à la transcriptase inverse, qui est utilisée conjointement avec Cas9 dans le prime editing, l’édition génomique a de nouveau été mise à niveau.
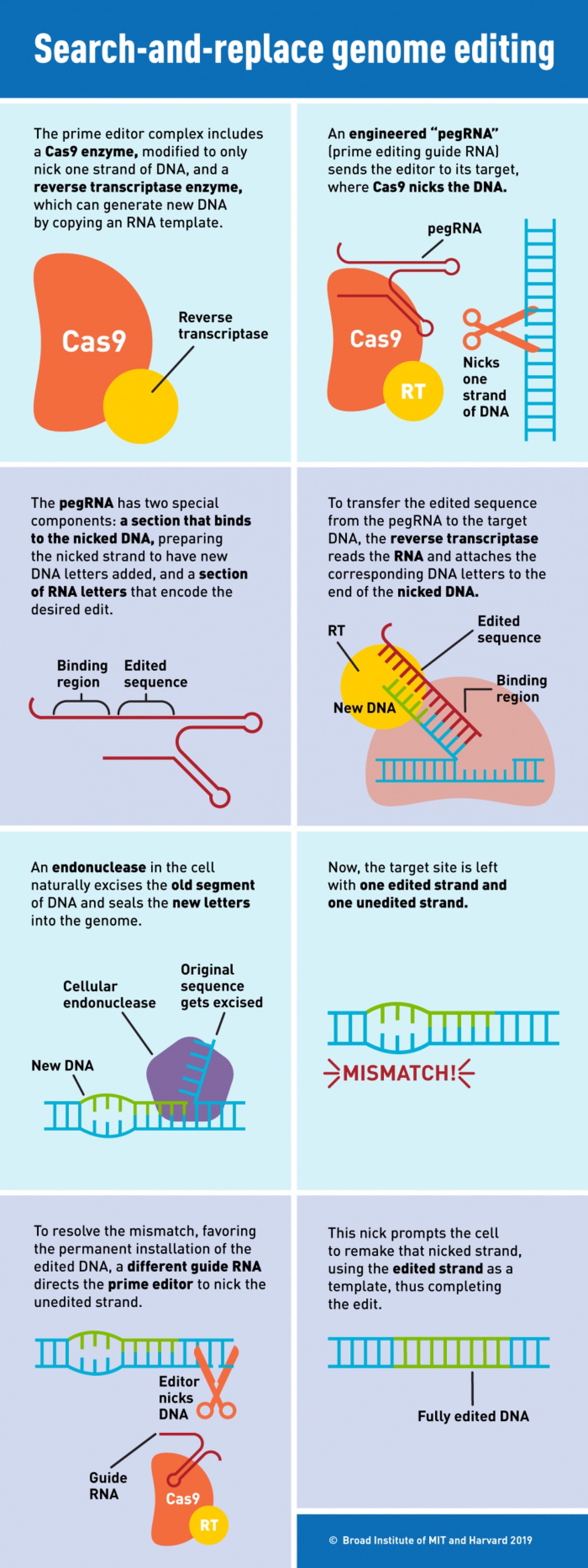
Dans cette nouvelle méthode d’édition génétique, un ARN guide appelé ARNpeg dirige une forme modifiée de l’enzyme Cas9 pour ne couper qu’un seul brin d’ADN (empêchant les ruptures de double brin qui peuvent provoquer des perturbations involontaires).
Ensuite, l’enzyme transcriptase inverse copie directement l’information génétique modifiée contenue dans le pegRNA vers le site génomique ciblé.
Une explication détaillée de la procédure dans l’infographie ci-dessous. (Broad Institute)
Selon Andrew Anzalone, biologiste chimiste au Broad Institute :
La polyvalence du prime editing est rapidement devenue évidente lorsque nous avons développé cette technologie.
Le fait que nous puissions copier directement de nouvelles informations génétiques dans un site cible a été une révélation. On était vraiment intéressé.
La flexibilité du système signifie que, pour la première fois, les chercheurs peuvent échanger efficacement une » lettre » d’ADN avec une autre, parmi l’adénine (A), cytosine (C), guanine (G), et thymine (T), dans les 12 voies possibles.
C’est une nette amélioration par rapport aux progrès réalisés par l’éditeur de base en 2017, ce qui signifie qu’il est maintenant possible d’apporter des modifications génétiques d’un genre entièrement nouveau dans les maladies humaines par rapport à ce qui pouvait être fait auparavant.
Selon Liu :
Avec le prime editing, nous pouvons maintenant corriger directement la mutation de la drépanocytose en rétablissant la séquence normale et en éliminant les quatre bases ADN supplémentaires qui causent la maladie de Tay Sachs, sans couper l’ADN entièrement ni avoir besoin de modèles ADN.
Dans la nouvelle étude des chercheurs, l’équipe détaille ces procédures dans des tests en laboratoire, parmi un compte rendu de plus de 175 vérifications dans des cellules humaines et de souris, avec des résultats qui ont produit moins de sous-produits indésirables et introduit moins de changement hors cible que la méthode Cas9 seule aurait permis de réaliser.
Il s’agit d’un événement marquant, mais surtout étant donné le rythme rapide auquel ces technologies évoluent, les chercheurs soulignent que nous n’en sommes encore qu’au début des essais du système, ils sont impatients de déterminer ce dont il est encore capable dans un environnement de laboratoire.
Selon les chercheurs dans leur étude :
Beaucoup de recherches supplémentaires sont nécessaires pour mieux comprendre et améliorer le prime editing dans un large éventail de types de cellules et d’organismes, pour évaluer cette méthode hors cible à l’échelle du génome et pour mieux caractériser la mesure dans laquelle le prime editing peut affecter les cellules.
Néanmoins, il est clair qu’il pourrait y avoir énormément de possibilités d’élargir l’échelle théorique et pratique de la révision du génome, en étendant la technique, en principe, à 89 % des variantes génétiques humaines pathogènes connues, d’après les chercheurs.
Les opportunités commerciales sont également potentiellement massives. Bien que les chercheurs accorderont à d’autres chercheurs une licence non commerciale pour explorer cette approche, les demandes commerciales pour le système en instance de brevet pourraient être plus que considérables pour ses inventeurs.
L’étude publiée dans Nature : Search-and-replace genome editing without double-strand breaks or donor DNA et présenyée sur le site du Broad Institute : New CRISPR genome editing system offers a wide range of versatility in human cells.

Pourquoi écrire « la Femme » pour parler d’Emmanuelle Charpentier ?