Des chercheurs trouvent un nouveau moyen d’extraire le CO2 des océans
Les océans absorbent d’énormes quantités de dioxyde de carbone, et des chercheurs du Massachusetts Institute of Technology (MIT/ États-Unis) affirment avoir mis au point un moyen de le libérer et de le capturer qui utilise beaucoup moins d’énergie que le captage direct dans l’air avec, en prime, quelques autres avantages environnementaux.
Image d’entête, à partir de l’étude : représentation d’un navire qui traiterait l’eau de mer au cours de leurs déplacements pour en éliminer le dioxyde de carbone. (S. Kim et col./ Energy & Environmental Science)
Extraire les gaz à effet de serre de l’eau est une idée étrange, mais les océans sont le premier puits de carbone de la planète, et le captage direct du carbone dans l’air présente de sérieux problèmes : il coûte cher et consomme beaucoup d’énergie. Selon les chiffres de l’Agence internationale de l’énergie (AIE) pour 2022, même les technologies de captage de l’air les plus efficaces nécessitent environ 6,6 gigajoules d’énergie, soit 1,83 mégawattheure par tonne de dioxyde de carbone capturé.
La majeure partie de cette énergie n’est pas utilisée pour séparer directement le CO2 de l’air, mais sous forme d’énergie thermique pour maintenir les absorbeurs à leur température de fonctionnement, ou d’énergie électrique pour comprimer de grandes quantités d’air jusqu’au point où l’opération de capture peut être effectuée efficacement. Mais dans tous les cas, les coûts sont hors de contrôle, avec des estimations de prix par tonne allant de 300 à 1 000 dollars en 2030. Aucune nation sur Terre n’est actuellement disposée à taxer les émetteurs de carbone à hauteur de la moitié de l’estimation la plus basse. La capture directe de l’air ne fonctionnera pas en tant qu’activité commerciale à moins que ses coûts ne baissent considérablement.
Il s’avère qu’il existe une autre option : l’eau de mer. Lorsque les concentrations de carbone dans l’atmosphère augmentent, le dioxyde de carbone commence à se dissoudre dans l’eau de mer. L’océan absorbe actuellement 30 à 40 % des émissions annuelles de carbone de l’humanité et maintient un échange libre constant avec l’air. En aspirant le carbone de l’eau de mer, il en aspirera davantage de l’air pour rééquilibrer les concentrations. Mieux encore, la concentration de dioxyde de carbone dans l’eau de mer est plus de 100 fois supérieure à celle de l’air.
Des équipes de recherche ont déjà réussi à libérer le CO2 de l’eau de mer et à le capturer, mais leurs méthodes nécessitaient des membranes coûteuses et un approvisionnement constant en produits chimiques pour maintenir les réactions en cours. L’équipe du MIT, en revanche, a annoncé le test réussi d’un système qui n’utilise ni l’un ni l’autre, et qui nécessite beaucoup moins d’énergie que les méthodes de capture de l’air.
Dans ce nouveau système, l’eau de mer passe par deux chambres. La première utilise des électrodes réactives pour libérer des protons dans l’eau de mer, ce qui acidifie cette dernière, transformant les bicarbonates inorganiques dissous en dioxyde de carbone gazeux, qui s’échappe sous forme de bulles et qui est recueilli par aspiration. L’eau est ensuite acheminée vers un deuxième ensemble de cellules à tension inversée, qui réintroduisent les protons et transforment l’eau acide en eau alcaline avant de la rejeter dans la mer. Périodiquement, lorsque l’électrode active est appauvrie en protons, la polarité de la tension est inversée, et la même réaction se poursuit avec l’eau qui circule dans la direction opposée.
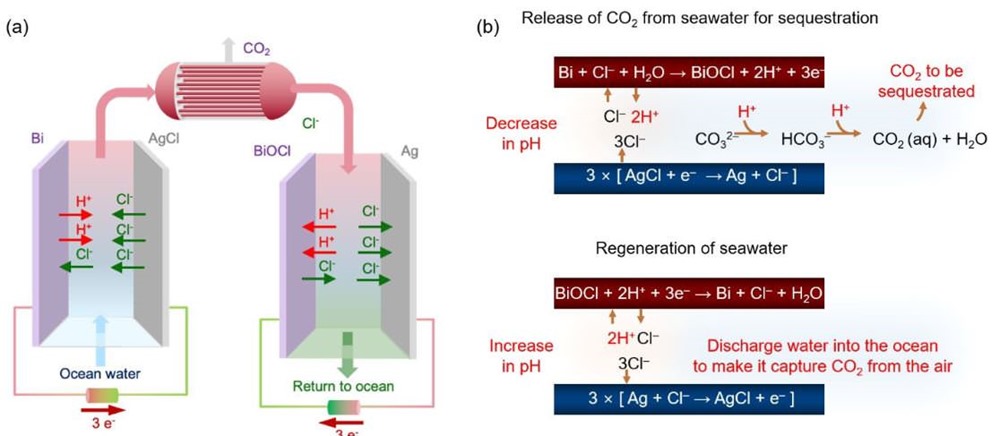
A partir de l’étude : (a) Principe général du système électrochimique médié par les chlorures pour l’élimination du CO2 de l’eau de mer. (b) Réactions électrochimiques à l’électrode de bismuth (rouge) et à l’électrode d’argent (bleu) à chaque étape, et libération ultérieure de CO2 dans l’eau océanique acidifiée. (S. Kim et col./ Energy & Environmental Science)
Dans une nouvelle étude (lien plus bas), l’équipe indique que sa technique nécessite un apport énergétique de 122 kJ/mol, ce qui équivaut à 0,77 mWh par tonne. Et l’équipe est convaincue qu’elle peut faire encore mieux, selon leur étude :
Bien que notre consommation d’énergie de base de 122 kJ/mol-CO2 constitue un record à la baisse, elle peut encore être considérablement réduite pour atteindre la limite thermodynamique de 32 kJ/mol-CO2.
L’équipe prévoit un coût optimisé d’environ 56 dollars (52 euros) par tonne de CO2 capturé, bien qu’il ne soit pas juste de le comparer directement aux coûts de capture directe de l’air dans un système complet. L’étude prévient que ces coûts ne comprennent pas le dégazage sous vide, la filtration et les « coûts auxiliaires extérieurs au système électrochimique », dont l’analyse devra être effectuée séparément. Certains de ces coûts pourraient toutefois être atténués en intégrant les unités de captage du carbone à d’autres installations, par exemple les usines de dessalement, qui traitent déjà de grands volumes d’eau de mer.
Il existe également d’autres avantages : l’accumulation accrue de carbone dans l’océan au cours des dernières années a déjà causé des problèmes d’acidification, menaçant les récifs coralliens et les coquillages. La production alcaline de ce processus, si elle est dirigée là où elle est nécessaire, pourrait contribuer à rétablir l’équilibre.
L’équipe a prévu de réaliser un projet de démonstration pratique au cours des deux prochaines années, et affirme qu’il y a encore beaucoup de choses à améliorer. Par exemple, les chercheurs aimeraient pouvoir séparer le gaz sans système à vide. De plus, des précipités minéraux encrassent les électrodes du côté de l’alcalinisation, ce qui signifie qu’il reste encore de nombreuses améliorations à apporter.
L’étude publiée dans la revue Energy & Environmental Science : Asymmetric chloride-mediated electrochemical process for CO2 removal from oceanwater et présentée sur le site du Massachusetts Institute of Technology : How to pull carbon dioxide out of seawater.